题目内容
7.治理环境污染、改善生态坏境已成为全人类的共识.①在煤中加入适从的石灰石作脱硫剂,可以减少硫酸型酸雨的发生.脱硫后产生的废料中含有的CaSO4(填化学式)可用于制造建筑材料.
②天然水中的杂质较多,常需加入明矾、氯化铁、漂白粉等处理后才能作为生活用水,氯化铁净水原理的离子方程式为Fe3++3H2O?Fe(OH)3(胶体)+3H+.漂白粉能杀菌消毒,其有效成分是Ca(ClO)2(填化学式).
③某工业废水中含有的铊(Tl+)具有高毒性,处理时常加入NaClO溶液,将 T1+转化为Tl3+,该反应中氧化剂是NaClO(填“T1+”或“NaClO”),同时加入适量氨水以调节水体的pH,从而将Tl3+转化为难溶的Tl(OH)3(填化学式)沉淀除去.
分析 ①煤和石油中的硫燃烧产生的二氧化硫是形成硫酸型酸雨的主要原因,通过脱硫可以减少硫酸型酸雨的产生;结合发生反应判断脱硫后产生的废料中可用于制造建筑材料的物质名称;
②氯化铁电离出的铁离子水解生成氢氧化铁胶体,能够净水;漂白粉的主要成分为氯化钙和次氯酸钙,有效成分为次氯酸钙;
③在废水中加入NaClO溶液,将Ti+转变为Ti3+,则NaClO中氯由+1价降低为-1价,为氧化剂;Tl3+与氨水反应生成Tl(OH)3沉淀.
解答 解:①在煤中加入适从的石灰石作脱硫剂,可以减少污染物SO2的排放,从而减少硫酸型酸雨的发生;碳酸钙与二氧化硫反应的方程式为:2CaCO3+2SO2+O2═2CaSO4+2CO2,所以脱硫后产生的废料中可用于制造建筑材料为CaSO4,
故答案为:硫酸;CaSO4;
②氯化铁电离出的铁离子发生水解反应Fe3++3H2O?Fe (OH)3(胶体)+3H+,生成的氢氧化铁胶体具有较大吸附面积,能够净水;
漂白粉的主要成分为CaCl2和Ca(ClO)2,其中Ca(ClO)2可生成具有氧化性的HOCl,可用于杀菌消毒,Ca(ClO)2为漂白粉的有效成分,
故答案为:Fe3++3H2O?Fe (OH)3(胶体)+3H+; Ca(ClO)2;
③某工业废水中含有的铊(Tl+)具有高毒性,处理时常加入NaClO溶液,将 T1+转化为Tl3+,该反应中NaClO中氯由+1价降低为-1价,所以氧化剂是NaClO;同时加入适量氨水以调节水体的pH,从而将Tl3+转化为难溶的 Tl(OH)3,
故答案为:NaClO;Tl(OH)3.
点评 本题考查较为综合,涉及污水处理、环境污染及治理、氧化还原反应等知识,题目难度中等,明确常见环境污染类型及治理方法为解答关键,试题有利于提高学生的环境保护意识.

| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
| A. | 元素X的常见化合价是+1价 | |
| B. | 若元素Y处于第3周期,它可与冷水剧烈反应 | |
| C. | 元素X与氯形成化合物时,化学式可能是XCl | |
| D. | 元素Y是ⅢA族的元素 |
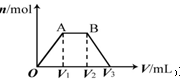 有KOH和Ca(OH)2的混合溶液,C(OH-)═0.1mol•L-1.取此溶液500mL,向其中通入CO2,通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示.图中(V1)为112mL(标准状况),则图中V2、V3的体积(单位为mL)分别是( )
有KOH和Ca(OH)2的混合溶液,C(OH-)═0.1mol•L-1.取此溶液500mL,向其中通入CO2,通入CO2的体积(V)和生成沉淀的物质的量(n)的关系如图所示.图中(V1)为112mL(标准状况),则图中V2、V3的体积(单位为mL)分别是( )| A. | 560、672 | B. | 1008、1120 | C. | 2240、2352 | D. | 392、504 |
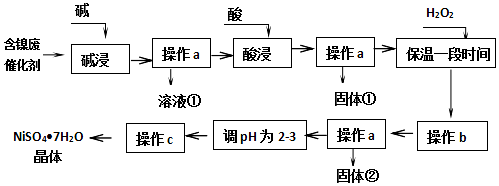
几种难溶碱开始沉淀和完全沉淀的pH:
| 沉淀物 | 开始沉淀 | 完全沉淀 |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
(1)溶液①中含金属元素的离子是AlO2-.
(2)用离子方程式表示加入双氧水的目的2Fe2++H2O2+2H+=2Fe3++2H2O.
双氧水可以用下列物质替代的是A.
A.氧气 B.漂白液 C.氯气 D.硝酸
(3)操作b调节溶液pH范围为3.2≤pH<7.1.
(4)操作a和c需要共同的玻璃仪器是玻璃棒.
上述流程中,防止浓缩结晶过程中Ni2+水解的措施是保持溶液呈酸性.
(5)如果加入双氧水量不足或“保温时间较短”,对实验结果的影响是产品中混有绿矾.操作c的名称:蒸发浓缩,冷却结晶.
| A. | Ca2+,Na+,NO3-,Cl- | B. | K+,Ba2+,Cl-,NO3- | ||
| C. | Na+,HCO3-,CO32-,K+ | D. | Na+,Cl-,K+,MnO4- |
(1)Cu2SO3•CuSO3•2H2O是一种深红色固体,不溶于水和乙醇,100℃时发生分解,其制备实验装置如图所示.
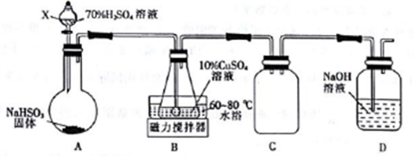
①仪器X的名称是分液漏斗.常温下用装置A制取SO2时,用较浓的硫酸而不用稀硫酸,其原因是SO2易溶于水,用较浓的硫酸有利于SO2的逸出.
②装置C的作用是防止倒吸.
③装置B中发生反应的离子方程式为3Cu2++3SO2+6H2O═Cu2SO3•CuSO3•2H2O↓+8H++SO42-.
④从装置B中获得的固体需先用蒸馏水充分洗涤,再真空干燥,而不直接用烘干的方式得到产品,其原因是防止Cu2SO3•CuSO3•2H2O发生分解和被氧化.
(2)向NaHSO3溶液中加入NaClO溶液时,反应有三种可能的情况:
I.NaHSO3和NaClO恰好反应;II.NaHSO3过量;III.NaClO过量.甲同学欲通过下列实验确定该反应属于哪一种情况,请完成表:
| 实验操作 | 预期现象及结论 |
| 取上述反应后的混合溶液于试管 A中,滴加稀硫酸 | 若有气泡产生,则①II(填“I”“II”或“III”,下同)成立,若没有气泡产生,则②I或III成立 |
| 另取上述反应后的混合溶液于试管B中,滴加几滴淀粉KI溶液,充分振荡 | ③溶液变为蓝色,则III成立 |