��Ŀ����
Ksp(AgCl)��1.56��10��10 ��Ksp(AgBr)��7.7��10��13,Ksp(Ag2CrO4)��9.0��10��12 ,��֪��ij��Һ�к���C1-, Br- ��CrO42-��Ũ�Ⱦ�Ϊ0.010mo1��L-�������Һ����μ���0.010mol��L-1��AgNO3��Һʱ�����������Ӳ����������Ⱥ�˳��Ϊ
A��C1- ��Br-��CrO42- B��CrO42-��Br-��C1-
C��Br-��C1-��CrO42- D��Br- ��CrO42-��C1-
C
��������
�����������������ʱ��AgCl��Һ��c��Ag+��= Ksp(AgCl)/ c��Cl-��=(1.56��10-10)/0.01=1.56��10-8mol/L��
AgBr��Һ��c��Ag+��= Ksp(AgBr)/ c��Cl-��=(7.7��10-13)/0.01mol/L=7.7��10-11mol/L��Ag2CrO4��Һ��c��Ag+��=[ Ksp(Ag2CrO4)/ c��CrO42-��]1/2=[(9.0��10-12)/0.01mol/L]1/2=3��10-5��c��Ag+��ԽС����Խ�����ɳ����������������Ӳ����������Ⱥ�˳��ΪBr-��Cl-��CrO42-��ѡC��
���㣺��������ܽ�ƽ�⡣

�ϳɰ������Ĵ����������˹��̵�����Ҫ;�������о�������ȷ������ָ�����ϳɰ���Ӧ��ƽ�ⳣ��Kֵ���¶ȵĹ�ϵ���£�
�¶ȣ��棩 | 360 | 440 | 520 |
Kֵ | 0.036 | 0.010 | 0.0038 |
��1����д����ҵ�ϳɰ��Ļ�ѧ����ʽ ��
�����ϱ����ݿ�֪�÷�ӦΪ���ȷ�Ӧ�������� ��
�������ϣ�Ϊ������ƽ��ʱH2��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�� ��������ţ�
a������ѹǿ b��ʹ�ú��ʵĴ���
c�������¶� d����ʱ����������е�NH3
��2��ԭ����H2��ͨ����Ӧ CH4(g) + H2O (g) CO(g) + 3H2(g) ��ȡ����֪�÷�Ӧ�У�����ʼ������е�
CO(g) + 3H2(g) ��ȡ����֪�÷�Ӧ�У�����ʼ������е� 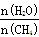 �㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ������ͼ��ʾ��
�㶨ʱ���¶ȡ�ѹǿ��ƽ������CH4������Ӱ������ͼ��ʾ��
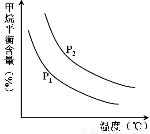
��ͼ�У��������߱�ʾѹǿ�Ĺ�ϵ�ǣ�P1 P2���>������=����<������
�ڸ÷�ӦΪ ��Ӧ������ȡ����ȡ�����
��3��ԭ����H2����ͨ����ӦCO(g) + H2O(g)  CO2 (g) + H2(g) ��ȡ��
CO2 (g) + H2(g) ��ȡ��
��T ��ʱ�����ݻ��̶�Ϊ5 L�������г���1 molˮ������1 mol CO����Ӧ��ƽ����CO��Ũ��Ϊ0.08 mol��L-1����ƽ��ʱCO��ת����Ϊ ���÷�Ӧƽ�ⳣ���ı���ʽΪ ��
�ڱ����¶���ΪT �棬�ı�ˮ������CO�ij�ʼ���ʵ���֮�ȣ������������з�Ӧ�����������ܹ�˵����ϵ����ƽ��״̬���� ������ţ���
a��������ѹǿ����ʱ��ı�
b�����������ܶȲ���ʱ��ı�
c����λʱ��������a mol CO2��ͬʱ����a mol H2
d���������n (CO) : n (H2O) : n (CO2) : n (H2) = 1 : 1 : 1 : 1
 CO��g��+H2��g���������ӷ�Ӧ�����ʵ���ʱ��ƽ��һ��������Ӧ�����ƶ�
CO��g��+H2��g���������ӷ�Ӧ�����ʵ���ʱ��ƽ��һ��������Ӧ�����ƶ�
 2Z(g),��X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3������Ϊ�㣩,��Ӧ�ﵽƽ��ʱ, X��Y��Z��Ũ�ȷֱ�Ϊ0.1mol/L��0.3 mol/L��0.08 mol/L�������жϲ���ȷ����
2Z(g),��X��Y��Z����ʼŨ�ȷֱ�Ϊc1��c2��c3������Ϊ�㣩,��Ӧ�ﵽƽ��ʱ, X��Y��Z��Ũ�ȷֱ�Ϊ0.1mol/L��0.3 mol/L��0.08 mol/L�������жϲ���ȷ����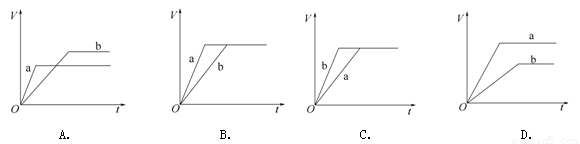
 2Fe(s) + 3CO(g) +6H2(g) �SH>0
2Fe(s) + 3CO(g) +6H2(g) �SH>0
 2NH3���ù����л�ԭ��Ӧ�ķ���ʽΪ ��
2NH3���ù����л�ԭ��Ӧ�ķ���ʽΪ ��
 )>c(OH
)>c(OH )> c(H+)
)> c(H+)