题目内容
3.下列判断错误的是( )| A. | 沸点:NH3>PH3>AsH3 | B. | 熔点:Si3N4>NaCl>Sil4 | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
分析 A、同一主族元素氢化物相对分子质量越大,其熔沸点越高,但含有氢键的氢化物熔沸点最高;
B、一般来说熔点:原子晶体>离子晶体>分子晶体;
C、元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
D、元素的金属越强,对应的最高价氧化物的水化物的碱性越强.
解答 解:A、同一主族元素氢化物相对分子质量越大,其熔沸点越高,但含有氢键的氢化物熔沸点最高,氨气中含有氢键,熔沸点最高,则熔沸点NH3>ASH3>PH3,故A错误;
B、一般来说熔点:原子晶体>离子晶体>分子晶体,所以熔点:原子晶体Si3N4>离子晶体NaCl>分子晶体Sil4,故B正确;
C、非金属性Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,所以酸性强弱顺序为:HClO4>H2SO4>H3PO4,故C正确;
D.金属性:Na>Mg>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性:NaOH>Mg(OH)2>Al(OH)3,故D正确.
故选A.
点评 本题考查元素周期表及元素周期律,为高频考点,把握元素的位置、性质及元素周期律为解答的关键,侧重性质比较的考查,题目难度不大.

练习册系列答案
 能力评价系列答案
能力评价系列答案
相关题目
4.化学与生活和生产密切相关,下列过程未涉及到化学变化的是( )
| A. | 皮肤被紫外线灼伤 | B. | NaHCO3药片做抗酸药 | ||
| C. | 甘油做护肤保湿剂 | D. | 供能剂MgH2为氢能源汽车提供H2 |
18.判断下列有关化学基本概念或名词的依据正确的是( )
| A. | 共价化合物:是否含有共价键 | |
| B. | 纯净物与混合物:是否仅含有一种元素 | |
| C. | 电解质与非电解质:物质本身是否具有导电性 | |
| D. | 溶液与胶体:本质在于分散质粒子直径的大小 |
15.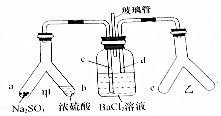 Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究.利用如图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件,下列判断正确的( )
Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究.利用如图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件,下列判断正确的( )
 Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究.利用如图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件,下列判断正确的( )
Y形管是一种特殊的仪器,与其他仪器组合可以进行某些实验探究.利用如图装置可以探究SO2与BaCl2反应生成BaSO3沉淀的条件,下列判断正确的( )| A. | 玻璃管的作用是连通大气,使空气中的氧气进人广口瓶,参与反应 | |
| B. | c、d两根导管郡必须插人BaCl2溶液中,保证气体与Ba2+充分接触 | |
| C. | Y形管乙中产生的为氧化性气体,将BaSO3氧化为BaSO4沉淀 | |
| D. | e、f两管中的试剂可以分别是浓氨水和NaOH |
12.标准状况下2.24LSO2与1L0.15mol•L-1的NaOH溶液反应,反应后溶液中的溶质是( )
| A. | NaHSO3 | B. | NaOH和Na2SO3 | C. | Na2SO3 | D. | Na2SO3和NaHSO3 |
13.在自然界中不存在游离态的元素是( )
| A. | 碳 | B. | 硫 | C. | 铁 | D. | 铝 |

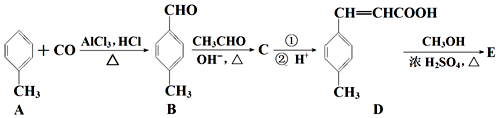
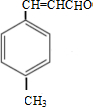 ;D→E的反应类型为酯化反应.
;D→E的反应类型为酯化反应.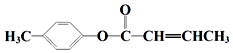 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为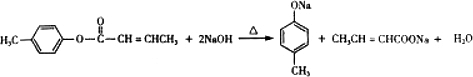 .
. .
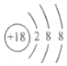
.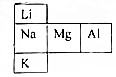 试分析它们的原子结构(电子层数、最外层电子)请指出:
试分析它们的原子结构(电子层数、最外层电子)请指出: