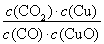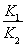题目内容
已知反应:CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
在427°C时的平衡常数是9.4.如果反应开始时,一氧化碳和水蒸气的浓度都是0.01mol·L-1,计算一氧化碳在此反应条件下的转化率。
75.4﹪
【解析】
试题分析:CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
起始:0.01mol/L 0.01mol/L 0 0
转化: x x x x
平衡0.01-x 0.01-x x x
依题意有: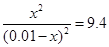 解之得:x=0.754mol
解之得:x=0.754mol
因此一氧化碳在此反应条件下的转化率为:
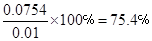
考点:考查平衡常数与转化率。

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案(8分)已知反应:CO(g) + H2O(g)H2(g) + CO2(g) ΔH= Q kJ·mol-1,其平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
请回答下列问题:
(1)上述可逆反应中Q 0(填“大于”或“小于”)。
(2)850℃时在体积为10L反应器中,通入一定量的CO和H2O(g)发生上述反应,CO和H2O(g)浓度变化如下图。试回答:
①0~4 min的平均反应速率v(CO)=______ mol/(L·min)
②下列表述能作为该可逆反应达到平衡标志的是__________(填序号)。
A.当混合气体的密度保持不变时
B.当反应消耗0.1molCO(g)同时也生成0.1molH2O(g)时
C.当CO(g)的质量分数保持不变时
D.当该反应的ΔH不变时
(3)若要加快该反应速率,同时还要提高CO的转化率,可采取的措施为_____(填序号)。
A.增加水蒸气的量 B.降低温度
C.使用催化剂 D.增大压强 E.不断移走CO2
(8分)已知反应:CO(g) + H2O(g) H2(g) + CO2(g) ΔH=" Q" kJ·mol-1,其平衡常数随温度的变化如下表:
H2(g) + CO2(g) ΔH=" Q" kJ·mol-1,其平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.9 4 4 | 9 | 1 |
(1)上述可逆反应中Q 0(填“大于”或“小于”)。
(2)850℃时在体积为10L反应器中,通入一定量的CO和H2O(g)发生上述反应,CO和H2O(g)浓度变化如下图。试回答:
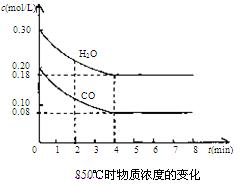
①0~4 min的平均反应速率v(CO)="______" mol/(L·min)
②下列表述能作为该可逆反应达到平衡标志的是__________(填序号)。
A.当混合气体的密度保持不变时
B.当反应消耗0.1molCO(g) 同时也生成0.1molH2O(g)时
C.当CO(g)的质量分数保持不变时
D.当该反应的ΔH不变时
(3)若要加快该反应速率,同时还要提高CO的转化率,可采取的措施为_____(填序号)。
A.增加水蒸气的量 B.降低温度
C.使用催化剂 D.增大压强 E.不断移走CO2
(8分)已知反应:CO(g) + H2O(g) H2(g) + CO2(g) ΔH= Q kJ·mol-1,其平衡常数随温度的变化如下表:
|
温度/℃ |
400 |
500 |
850 |
|
平衡常数 |
9.94 |
9 |
1 |
请回答下列问题:
(1)上述可逆反应中Q 0(填“大于”或“小于”)。
(2)850℃时在体积为10L反应器中,通入一定量的CO和H2O(g)发生上述反应,CO和H2O(g)浓度变化如下图。试回答:
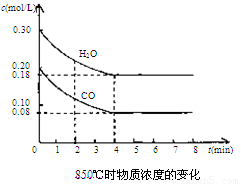
①0~4 min的平均反应速率v(CO)=______ mol/(L·min)
②下列表述能作为该可逆反应达到平衡标志的是__________(填序号)。
A.当混合气体的密度保持不变时
B.当反应消耗0.1molCO(g) 同时也生成0.1molH2O(g)时
C.当CO(g)的质量分数保持不变时
D.当该反应的ΔH不变时
(3)若要加快该反应速率,同时还要提高CO的转化率,可采取的措施为_____(填序号)。
A.增加水蒸气的量 B.降低温度
C.使用催化剂 D.增大压强 E.不断移走CO2