题目内容
13.现有 CnH2n 和CH3COOH 的混合物,若其中氧的质量分数为a%,则其中碳元素的质量分数为( )| A. | a% | B. | $\frac{3}{4}$a% | C. | $\frac{6(1-a%)}{7}$ | D. | $\frac{12(1-a%)}{13}$ |
分析 酸的化学式为C2H4O2,分子式为CnH2n,则在混合物中C、H原子数目之比为1:2,则C、H元素质量之比=12:2=6:1,混合物中一共有三种元素,氧的质量分数为a,则碳、氢元素的质量分数之和为1-a,然后根据C、H元素质量之比可计算出碳元素的质量分数.
解答 解:乙酸的化学式为C2H4O2,分子式为CnH2n,则在混合物中C、H原子数目之比为1:2,则C、H元素质量之比=12:2=6:1,混合物中一共有三种元素,氧的质量分数为a,则碳、氢元素的质量分数之和为1-a%,则化合物中碳元素质量分数=(1-a%)×$\frac{6}{6+1}$=$\frac{6(1-a%)}{7}$,故选C.
点评 本题考查混合物中元素质量分数计算,涉及化学式的有关计算,关键是根据化学式确定混合物中碳、氢的固定组成,较好的训练学生分析问题、解决问题的能力.

练习册系列答案
相关题目
4.NA表示阿伏加德罗常数,下列判断正确的是( )
| A. | 在 16g18O2中含有NA个氧原子 | |
| B. | 16gCH4中含有4NA个C-H 键 | |
| C. | 22g 某气体含分子数为 0.5NA,则其摩尔质量为 44 | |
| D. | 含 NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为 1 mol•L-1 |
1.现有结构式为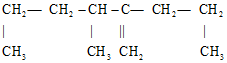 有机物,其正确命名应是( )
有机物,其正确命名应是( )
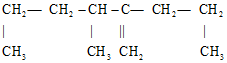 有机物,其正确命名应是( )
有机物,其正确命名应是( )| A. | 2,3-二丙基-1-丁烯 | B. | 2-丙基-3,5-二甲基-1-戊烯 | ||
| C. | 3-甲基-2-丙基-1-己烯 | D. | 3,5-二甲基-2-丙基-1-戊烯 |
8.将一定体积的SO3(g)充入恒容的密闭容器中,发生反应2SO3(g)?2SO2(g)+O2(g)并达到平衡;保持温度不变,再充入相同体积的SO3(g),达到新平衡后,与原平衡相比,下列值减小的是( )
| A. | 平均相对分子质量 | B. | SO3(g)的转化率 | ||
| C. | $\frac{c(S{O}_{3})}{c(S{O}_{2})}$ | D. | c2(SO3) |
5.标况下H2S和O2的混合气体200毫升,经点燃反应至完全,所得气体经干燥后,恢复至标况体积为20毫升,该20毫升气体可能是( )
| A. | H2S和SO2 | B. | O2 | C. | H2S | D. | SO3 |
2.向Fe和Al2O3的混合物中加入足量稀硫酸将其溶解,室温下向所得溶液中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
| A. | 通入过量的氨气:NH4+、SO42-、Na+、AlO2- | |
| B. | 加入过量NaHCO3溶液:SO42-、Na+、Al3+、HCO3-、Fe2+ | |
| C. | 加入过量氯水:Cl-、SO42-、Fe3+、Al3+ | |
| D. | 加入过量NaNO3溶液:NO3-、SO42-、Fe2+、Al3+、Na+ |
3.下列关于有机化合物的说法正确的是( )
| A. | 戊烷有4种同分异构体 | |
| B. | 乙酸和溴乙烷均可发生加成反应 | |
| C. | 乙烷和乙烯可用酸性KMnO4溶液鉴别 | |
| D. | 皂化反应的产物是高级脂肪酸和甘油 |