题目内容
对氮及其化合物的研究具有重要意义.

(1)在1L密闭容器中,4mol氨气在一定条件下分解生成氮气和氢气.2min时反应吸收热量为46.1kJ,此时氨气的转化率为25%.该反应的热化学方程式为 ,这段时间内v(H2)= .
(2)298K时.在2L固定体积的密闭容器中,发生可逆反应:2NO2(g)fN2O4(g)△H=-akJ?mol-1(a>0),N2O4的物质的量浓度随时间变化如图1所示.达平衡时,N2O4的浓度为NO2的2倍.
①298K时,该反应的化学平衡常数为 (精确到0.01);
②下列情况不是处于平衡状态的是 (填字母序号);
a.混合气体的密度保持不变
b.混合气体的颜色不再变化
e.气压恒定时
③若反应在398K进行,某时刻测得n(NO2)=0.6mol,n(N2O4)=1.2mol,则此时v正 v逆(填“>”、“<”或“=”).
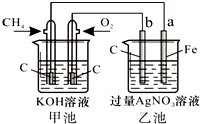
(3)用氨气可设计成如图2所示燃料电池,产生的X气体可直接排放到大气中.则a电极电极反应式为 .
(4)t℃下,某研究人员测定NH3?H2O的电离常数为1.8×10-5.NH4+的水解常数为1.5×10-8,则该温度下水的离子积常数为 ,请判断t 25℃(填“>”、“<”或“=”).

(1)在1L密闭容器中,4mol氨气在一定条件下分解生成氮气和氢气.2min时反应吸收热量为46.1kJ,此时氨气的转化率为25%.该反应的热化学方程式为
(2)298K时.在2L固定体积的密闭容器中,发生可逆反应:2NO2(g)fN2O4(g)△H=-akJ?mol-1(a>0),N2O4的物质的量浓度随时间变化如图1所示.达平衡时,N2O4的浓度为NO2的2倍.
①298K时,该反应的化学平衡常数为
②下列情况不是处于平衡状态的是
a.混合气体的密度保持不变
b.混合气体的颜色不再变化
e.气压恒定时
③若反应在398K进行,某时刻测得n(NO2)=0.6mol,n(N2O4)=1.2mol,则此时v正
(3)用氨气可设计成如图2所示燃料电池,产生的X气体可直接排放到大气中.则a电极电极反应式为
(4)t℃下,某研究人员测定NH3?H2O的电离常数为1.8×10-5.NH4+的水解常数为1.5×10-8,则该温度下水的离子积常数为
考点:化学平衡的计算,原电池和电解池的工作原理,化学平衡状态的判断,弱电解质在水溶液中的电离平衡
专题:
分析:(1)4mol氨气在一定条件下分解生成氮气和氢气,2min时反应吸收热量为46.1kJ,此时氨气的转化率为25%,即分解1mol氨气吸收热量是46.1kJ,据热化学方程式的意义以及v=
来计算回答;
(2)①有图可知N2O4的平衡浓度为0.6mol/L,达到平衡时,N2O4的浓度为NO2的2倍,则NO2的平衡浓度为0.3mol/L,带入平衡常数表达式计算;
②a、气体的质量不变,容积恒定,因此气体的密度为一定值;
b、混合气体的颜色不变说明NO2的浓度保持恒定;
c、反应2NO2(g)?N2O4(g)气压恒定时,正、逆反应速率相等;
③反应为放热反应,升高温度,K值减小,计算可知此时的浓度商Q=K(298K)>K(398K),反应向逆反应方向移动,因此V(正)<V(逆);
(3)氨气作燃料应充入负极区,碱性燃料电池氢氧根离子常参与电极反应;
(4)氨气中的N失去电子化合价升高,由于X无污染可以确定X为氮气,根据Kw=Kh×Kb代入计算即可,Kw与温度成正比,以此判断T与25℃的大小.
| △c |
| △t |
(2)①有图可知N2O4的平衡浓度为0.6mol/L,达到平衡时,N2O4的浓度为NO2的2倍,则NO2的平衡浓度为0.3mol/L,带入平衡常数表达式计算;
②a、气体的质量不变,容积恒定,因此气体的密度为一定值;
b、混合气体的颜色不变说明NO2的浓度保持恒定;
c、反应2NO2(g)?N2O4(g)气压恒定时,正、逆反应速率相等;
③反应为放热反应,升高温度,K值减小,计算可知此时的浓度商Q=K(298K)>K(398K),反应向逆反应方向移动,因此V(正)<V(逆);
(3)氨气作燃料应充入负极区,碱性燃料电池氢氧根离子常参与电极反应;
(4)氨气中的N失去电子化合价升高,由于X无污染可以确定X为氮气,根据Kw=Kh×Kb代入计算即可,Kw与温度成正比,以此判断T与25℃的大小.
解答:
解:(1)4mol氨气在一定条件下分解生成氮气和氢气,2min时反应吸收热量为46.1kJ,此时氨气的转化率为25%,即分解1mol氨气吸收热量是46.1kJ,据热化学方程式的意义,反应的热化学方程式为:2NH3(g)?N2(g)+3H2(g)△H=+92.2kJ/mol,消耗1mol氨气会生成氢气1.5mol,体积是1L,所以v(H2)=
=0.75mol/(L?min),故答案为:2NH3(g)?N2(g)+3H2(g)△H=+92.2kJ/mol;0.75mol/(L?min);
(2))①有图可知N2O4的平衡浓度为0.6mol/L,达到平衡时,N2O4的浓度为NO2的2倍,则NO2的平衡浓度为0.3mol/L,则K=
=
=6.67L/mol,
故答案为:6.67;
②a、反应物和生成物全是气态物质,气体的质量不变,容积为2L保持恒定,由ρ=
可知气体的密度为一定值,因此气体的密度保持不变不一定处于平衡状态,故a选;
b、混合气体的颜色不变说明NO2的浓度不变,说明反应处于化学平衡状态,故b不选;
c、反应2NO2(g)?N2O4(g)是一个气体体积减小的反应,气压恒定时,正、逆反应速率相等,说明反应处于化学平衡状态,故c不选;
故答案为:a;
③反应为放热反应,升高温度,K值减小,密闭容器的体积为2L,因此的N2O4的浓度为0.6mol/L,NO2的浓度为0.3mol/L,浓度商Q=
=
=6.67L/mol=K(298K)>K(398K),反应向逆反应方向移动,因此V(正)<V(逆);
故答案为:<;
(3)在燃料电池中,可燃物充入负极区,所以NH3充入的a极作负极,产生的X气体为氧化产物,可直接排放到大气中,说明X对大气无污染,因此X为氮气,由该燃料电池示意图可知负极反应产物有水,由于是碱性电池,氢氧根离子也参与负极电极反应,综上所述可写出负极反应式:2NH3+6OH--6e-=N2+6H2O;
故答案为:2NH3+6OH--6e-=N2+6H2O;
(4)根据公式Kw=Kh×Kb,T℃下Kw=1.5×10-8×1.8×10-5=2.7×10-13;水的电离是吸热的,所以温度越高Kw越大,由于2.7×10-13>1.0×10-14,所以T>25℃,
故答案为:2.7×10-13;>.
| 1.5mol/L |
| 2min |
(2))①有图可知N2O4的平衡浓度为0.6mol/L,达到平衡时,N2O4的浓度为NO2的2倍,则NO2的平衡浓度为0.3mol/L,则K=
| c(N2O4) |
| c2(NO2) |
| 0.6mol/L |
| (0.3mol/L)2 |
故答案为:6.67;
②a、反应物和生成物全是气态物质,气体的质量不变,容积为2L保持恒定,由ρ=
| m |
| V |
b、混合气体的颜色不变说明NO2的浓度不变,说明反应处于化学平衡状态,故b不选;
c、反应2NO2(g)?N2O4(g)是一个气体体积减小的反应,气压恒定时,正、逆反应速率相等,说明反应处于化学平衡状态,故c不选;
故答案为:a;
③反应为放热反应,升高温度,K值减小,密闭容器的体积为2L,因此的N2O4的浓度为0.6mol/L,NO2的浓度为0.3mol/L,浓度商Q=
| c(N2O4) |
| c2(NO2) |
| 0.6mol/L |
| (0.3mol/L)2 |
故答案为:<;
(3)在燃料电池中,可燃物充入负极区,所以NH3充入的a极作负极,产生的X气体为氧化产物,可直接排放到大气中,说明X对大气无污染,因此X为氮气,由该燃料电池示意图可知负极反应产物有水,由于是碱性电池,氢氧根离子也参与负极电极反应,综上所述可写出负极反应式:2NH3+6OH--6e-=N2+6H2O;
故答案为:2NH3+6OH--6e-=N2+6H2O;
(4)根据公式Kw=Kh×Kb,T℃下Kw=1.5×10-8×1.8×10-5=2.7×10-13;水的电离是吸热的,所以温度越高Kw越大,由于2.7×10-13>1.0×10-14,所以T>25℃,
故答案为:2.7×10-13;>.
点评:本题考查知识点全面,涉及热化学方程式的书写、平衡常数的计算、平衡的移动、等知识点,难度中等.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
下列分子中的碳原子一定处于同一平面的是( )
A、 |
B、 |
| C、CH≡CCH2CH3 |
| D、CH3CH=CHCHO |
下列含有非极性键的共价化合物是( )
| A、H2O2 |
| B、Na2O2 |
| C、HCl |
| D、CH4 |
海洋中有丰富的食品、矿产、能源、药物和水产资源,如图为海水利用的部分过程.下列有关说法正确的是( )


| A、工业上一般用电解熔融MgO来制取金属镁 |
| B、海水中还含有碘元素,只需将海水中的碘升华就可以得到碘单质 |
| C、在第③、④、⑤步骤中,溴元素均被氧化 |
| D、从海水中得到的NaCl也是制造化肥NH4Cl的原料 |
 如图,根据所学知识填空:
如图,根据所学知识填空: