题目内容
实验室需要0.2mol/L CuSO4溶液250mL,实验室可提供配制溶液的试剂有:①蓝色胆矾晶体(CuSO4?5H2O) ②白色无水CuSO4③5mol/L CuSO4溶液
(1)无论采用何种试剂进行配制,实验必须用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还需要
(2)若用胆矾晶体进行配制,需用托盘天平称取CuSO4?5H2O的质量为 g;如果用5mol/L的CuSO4溶液稀释配制,需用量筒量取 ml 5mol/L CuSO4溶液.
(3)实验室用5mol/L的硫酸铜溶液稀释配制溶液所需的实验步骤有:其中正确的操作顺序为
①往烧杯中加入约100ml水进行初步稀释
②用量筒量取一定体积5mol/L 的硫酸铜溶液于一烧杯
③计算所需5mol/L 硫酸铜溶液的体积
④将溶液颠倒摇匀后转存于试剂瓶
⑤加水至液面离容量瓶1-2cm处改用胶头滴管进行定容
⑥洗涤烧杯和玻璃棒2-3次并将洗涤液注入容量瓶
⑦将溶液转移入容量瓶
⑧振荡摇匀
(4)配制溶液过程中,如果出现以下情况,对结果有何影响(填“偏高”、“偏低”、“无影响”)
A.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
B.定容时俯视刻度线
C.容量瓶未干燥即用来配制溶液 .
(1)无论采用何种试剂进行配制,实验必须用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还需要
(2)若用胆矾晶体进行配制,需用托盘天平称取CuSO4?5H2O的质量为
(3)实验室用5mol/L的硫酸铜溶液稀释配制溶液所需的实验步骤有:其中正确的操作顺序为
①往烧杯中加入约100ml水进行初步稀释
②用量筒量取一定体积5mol/L 的硫酸铜溶液于一烧杯
③计算所需5mol/L 硫酸铜溶液的体积
④将溶液颠倒摇匀后转存于试剂瓶
⑤加水至液面离容量瓶1-2cm处改用胶头滴管进行定容
⑥洗涤烧杯和玻璃棒2-3次并将洗涤液注入容量瓶
⑦将溶液转移入容量瓶
⑧振荡摇匀
(4)配制溶液过程中,如果出现以下情况,对结果有何影响(填“偏高”、“偏低”、“无影响”)
A.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
B.定容时俯视刻度线
C.容量瓶未干燥即用来配制溶液
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)依据配制一定物质的量浓度溶液步骤选择需要仪器;
(2)依据m=CVM计算需要溶质的质量;依据稀释前后溶质的物质的量不变计算需要硫酸铜的体积,依据硫酸铜体积选择量筒规格;
(3)依据配制一定物质的量浓度溶液步骤排序;
(4)分析不当操作对溶质的物质的量和溶液的体积的影响,依据C=
进行误差分析.
(2)依据m=CVM计算需要溶质的质量;依据稀释前后溶质的物质的量不变计算需要硫酸铜的体积,依据硫酸铜体积选择量筒规格;
(3)依据配制一定物质的量浓度溶液步骤排序;
(4)分析不当操作对溶质的物质的量和溶液的体积的影响,依据C=
| n |
| V |
解答:
解:(1)配制一定物质的量浓度溶液步骤有:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等,用到的仪器有:托盘天平、药匙、烧杯、玻璃棒
250mL容量瓶、胶头滴管,
故答案为:250mL容量瓶;
(2)配制0.2mol/L CuSO4溶液250mL,需要CuSO4?5H2O的质量m=0.2mol/L×0.25L×250g/mol=12.5g;
如果用5mol/L的CuSO4溶液稀释配制,设需要浓硫酸铜溶液的体积为V,依据稀释前后溶质的物质的量不变,5mol/L×V=0.2mol/L×250mL,
解得V=10.0ml,所以应选择10ml量筒;
故答案为:12.5;10;
(3)用浓溶液配制一定物质的量浓度溶液步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,所以正确的顺序为:③②①⑦⑥⑧⑤④;
故答案为:③②①⑦⑥⑧⑤④;
(4)A.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线,导致溶液的体积偏大,溶液的浓度偏低;
故答案为:偏低;
B.定容时俯视刻度线,导致溶液的体积偏小,溶液的浓度偏高;
故答案为:偏高;
C.容量瓶未干燥即用来配制溶液,对溶质的物质的量和溶液的体积都不会产生影响,溶液的浓度不变;
故答案为:无影响.
250mL容量瓶、胶头滴管,
故答案为:250mL容量瓶;
(2)配制0.2mol/L CuSO4溶液250mL,需要CuSO4?5H2O的质量m=0.2mol/L×0.25L×250g/mol=12.5g;
如果用5mol/L的CuSO4溶液稀释配制,设需要浓硫酸铜溶液的体积为V,依据稀释前后溶质的物质的量不变,5mol/L×V=0.2mol/L×250mL,
解得V=10.0ml,所以应选择10ml量筒;
故答案为:12.5;10;
(3)用浓溶液配制一定物质的量浓度溶液步骤:计算、量取、稀释、冷却、移液、洗涤、定容、摇匀等,所以正确的顺序为:③②①⑦⑥⑧⑤④;
故答案为:③②①⑦⑥⑧⑤④;
(4)A.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线,导致溶液的体积偏大,溶液的浓度偏低;
故答案为:偏低;
B.定容时俯视刻度线,导致溶液的体积偏小,溶液的浓度偏高;
故答案为:偏高;
C.容量瓶未干燥即用来配制溶液,对溶质的物质的量和溶液的体积都不会产生影响,溶液的浓度不变;
故答案为:无影响.
点评:本题考查了配制一定物质的量浓度的溶液的方法,明确配制原理是解题关键,注意量筒、容量瓶规格的选择依据.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质不能通过化合反应制得的是( )
| A、Fe(OH)2 |
| B、Fe(OH)3 |
| C、CaSiO3 |
| D、Fe(NO3)3 |
下列有关说法正确的是( )
| A、氯化钠溶液均一稳定透明,不是分散系 |
| B、冰水混合物是一种分散系 |
| C、分散系有的是纯净物有的是混合物 |
| D、分散系都是混合物,按分散质和分散剂所处的状态,分散系的组合有9种方式 |
下列分离物质的方法正确的是( )
| A、用萃取的方法除去花生油中的水份 |
| B、用过滤的方法除去NaCl溶液中含有的少量淀粉 |
| C、用酒精萃取碘水中的碘 |
| D、用蒸馏的方法除去水中的不挥发的杂质 |
0.06mol Cu投入到一定量的浓HNO3中,Cu完全溶解,将生成的NO2和NO气体全部收集到一试管中,然后将此试管倒扣装有水的水槽中,向此试管中缓慢通入标准状况下一定体积的O2,最终恰好使溶液充满整个试管,则通入O2的体积为( )
| A、896 mL |
| B、672 mL |
| C、560 mL |
| D、448 mL |
下列叙述正确的是( )
| A、c(NH4+)相等的(NH4)2SO4、(NH4)2Fe(SO4)2和NH4Cl溶液中,溶质浓度大小关系是:c[(NH4)2Fe(SO4)2]<c[(NH4)2SO4]<c(NH4Cl) |
| B、pH相同的盐酸和醋酸稀释相同倍数后,盐酸的pH小于醋酸的pH |
| C、中和体积与pH都相同的盐酸和醋酸所消耗的NaOH物质的量相同 |
| D、CH3COONa溶液中:c(Na+)=c(CH3COO-)+c(OH-)-c(H+) |


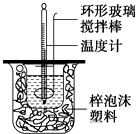 用50mL 0.50mol?L-1的盐酸与50mL 0.55mol?L-1的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题.
用50mL 0.50mol?L-1的盐酸与50mL 0.55mol?L-1的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题.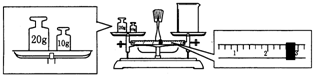 实验室欲用NaOH固体配制1.0mol?L-1的NaOH溶液240mL:
实验室欲用NaOH固体配制1.0mol?L-1的NaOH溶液240mL: