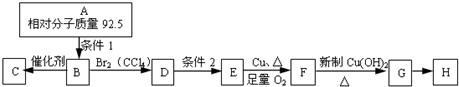
题目内容
某实验小组用0.50mol?L-1 NaOH溶液和0.55mol?L-1盐酸溶液进行中和热的测定.配制0.50mol?L-1 NaOH溶液
(1)若实验中要使用250mL NaOH溶液,至少需要称量NaOH固体 g.
(2)配制250mL0.50mol?L-1 NaOH固体所需要的玻璃仪器(填字母): .
A.量筒 B.烧杯 C.玻璃棒 D.胶头滴管 E.250mL容量瓶.
(1)若实验中要使用250mL NaOH溶液,至少需要称量NaOH固体
(2)配制250mL0.50mol?L-1 NaOH固体所需要的玻璃仪器(填字母):
A.量筒 B.烧杯 C.玻璃棒 D.胶头滴管 E.250mL容量瓶.
考点:中和热的测定
专题:实验题
分析:(1)根据公式m=nM=cVM来计算氢氧化钠的质量;
(2)根据各仪器的作用选取仪器.
(2)根据各仪器的作用选取仪器.
解答:
解:(1)需要称量NaOH固体m=nM=cVM=0.5mol/L×0.25L×40g/mol=5.0g,故答案为:5.0;
(2)用烧杯溶解NaOH,用玻璃棒搅拌和引流,用250mL容量瓶配制溶液,用胶头滴管定容,所以所需要的玻璃仪器有:烧杯、玻璃棒、胶头滴管、250mL容量瓶;
故答案为:BCDE.
(2)用烧杯溶解NaOH,用玻璃棒搅拌和引流,用250mL容量瓶配制溶液,用胶头滴管定容,所以所需要的玻璃仪器有:烧杯、玻璃棒、胶头滴管、250mL容量瓶;
故答案为:BCDE.
点评:本题考查中和热的测定,题目难度大,注意理解中和热的概念、步骤仪器等.

练习册系列答案
相关题目
电解质溶液有许多奇妙之处,你只有深入思考,才能体会到它的乐趣.下列关于电解质溶液的叙述中正确的是( )
| A、Na2CO3、NaHCO3两种盐溶液中,离子种类不相同 |
| B、常温下,1 mol?L-1的CH3COOH溶液与1 mol?L-1的NaOH溶液等体积混合后,所得混合液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| C、将AlCl3溶液加热蒸干并灼烧后剩余固体为Al2O3 |
| D、常温下,某溶液中由水电离出的c(H+)=10-5 mol?L-1,则此溶液可能是盐酸 |
下列属于化学变化的是( )
| A、氯气使淀粉碘化钾试纸变蓝 |
| B、溴易溶于四氯化碳 |
| C、氯化钠焰色反应呈黄色 |
| D、食盐水能导电 |
下列萃取与分液结合进行的操作(用CCl4为萃取剂从碘水中萃取碘)中错误的是( )
| A、饱和碘水和CCl4加入分液漏斗中后,塞上上口部的玻璃塞,用右手压住分液漏斗上口部,左手握住活塞部分,把分液漏斗倒转过来振荡 |
| B、静置,分液漏斗中溶液分层,下层呈紫红色上层几乎无色 |
| C、打开分液漏斗的活塞使下层液体沿烧杯内壁慢慢流出 |
| D、下层液体流完后继续打开活塞另用容器接收上层液体 |
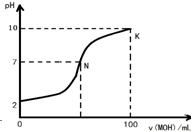 常温下,向l00mL 0.01mol?L-1 盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )
常温下,向l00mL 0.01mol?L-1 盐酸中逐滴加入0.02mol?L-1 MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中不正确的是( )| A、MOH是弱碱 | ||
| B、N点c(Cl-)=c(M+) | ||
| C、K点对应的溶液c(MOH)+c(OH-)-c(H+)=0.001 mol?L-1 | ||
D、随着MOH溶液的滴加,比值
|
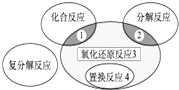
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )

A、2H2+O2
| ||||
| B、Zn+H2SO4=ZnSO4+H2↑ | ||||
C、CuO+CO
| ||||
D、2NaHCO3
|