题目内容
下列离子方程式中正确的是( )
| A、铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
| B、Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑ |
| C、硫酸铜与Ba(OH)2溶液反应:Cu2++2OH-=Cu(OH)2↓ |
| D、实验室用大理石和稀盐酸制取CO2:2H++CaCO3═Ca2++CO2↑+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.铁和稀硫酸反应生成亚铁盐;
B.原子不守恒;
C.二者反应还生成硫酸钡沉淀;
D.大理石和盐酸反应生成可溶性盐、二氧化碳和水.
B.原子不守恒;
C.二者反应还生成硫酸钡沉淀;
D.大理石和盐酸反应生成可溶性盐、二氧化碳和水.
解答:
解:A.铁和稀硫酸反应生成亚铁盐,离子方程式为Fe+2H+═Fe2++H2↑,故A错误;
B.原子不守恒,离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑,故B错误;
C.二者反应还生成硫酸钡沉淀,离子方程式为Cu2++2OH-+Ba2++SO42-=BaSO4↓+Cu(OH)2↓,故C错误;
D.大理石和盐酸反应生成可溶性盐、二氧化碳和水,离子方程式为2H++CaCO3═Ca2++CO2↑+H2O,故D正确;
故选D.
B.原子不守恒,离子方程式为2Na2O2+2H2O=4Na++4OH-+O2↑,故B错误;
C.二者反应还生成硫酸钡沉淀,离子方程式为Cu2++2OH-+Ba2++SO42-=BaSO4↓+Cu(OH)2↓,故C错误;
D.大理石和盐酸反应生成可溶性盐、二氧化碳和水,离子方程式为2H++CaCO3═Ca2++CO2↑+H2O,故D正确;
故选D.
点评:本题考查了离子方程式的书写,明确离子方程式书写规则是解本题关键,要遵循客观事实、原子守恒、电荷守恒和转移电子守恒,有的离子反应还与反应物的量有关,为易错点.

练习册系列答案
相关题目
下列说法中不正确的是( )
| A、在标准状况下22.4LH2中含有的氢分子的个数为NA |
| B、1L1mol/L的KClO3溶液中含有的Cl-个数为NA |
| C、凡是溶于水能导电的化合物就是电解质 |
| D、某溶液中滴加烧碱溶液,加热产生能使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定存在NH4+ |
下列实验、现象与结论不一致的是( )
| 选项 | A | B | C | D |
| 实验 | 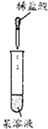 | 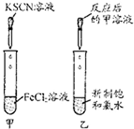 |  | 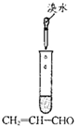 |
| 现象 | 出现白色沉淀 | 甲、乙中溶液均未变红 | 苯中不褪色,甲苯在褪色 | 溶液褪色 |
| 结论 | 原溶液可能含Ag+或SiO32- | 氯水可能氧化SCN- | 甲苯中甲基易被氧化 | 可证明分子中含碳碳双建 |
| A、A | B、B | C、C | D、D |
盐酸与碳酸钠固体反应时,能使反应的最初速率明显加快的是( )
| A、增加碳酸钠固体的量 |
| B、盐酸的量增加一倍 |
| C、盐酸的用量加倍浓度减半 |
| D、温度升高40℃ |
用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A、32g氧气和28g CO和N2的混合气体,含为原子数目相等 |
| B、等物质的量浓度的盐酸和硫酸,H+的物质的量浓度相等 |
| C、在常温常压下,11.2L氯气的分子数为0.5NA |
| D、把40g NaOH固体溶于1L水中,所得NaOH溶液的物质的量浓度为1mol?L-1 |
已知:(1)A、C均能与稀 H2SO4反应放出气体;(2)B与D的硝酸盐反应,置换出单质D;(3)C与强碱反应放出气体;(4)C、E在冷浓H2SO4中发生钝化反应,由此可以推断A、B、C、D、E依次为( )
| A、Fe、Cu、Al、Ag、Mg |
| B、Al、Cu、Mg、Ag、Fe |
| C、Mg、Cu、Al、Ag、Fe |
| D、Mg、Ag、Al、Cu、Fe |