题目内容
10.下列判断不正确的是( )| A. | 微粒半径:S2->K+>F- | |
| B. | 沸点:HCl<HF | |
| C. | 反应速率:Fe加入稀H2SO4中<Fe加入稀H2SO4和含少量CuSO4的混合溶液中 | |
| D. | 给出质子的能力:CH3COOH>C2H5OH>H2O |
分析 A.电子层越多,离子半径越大;具有相同电子排布的离子,原子序数大的离子半径小;
B.HF分子间含氢键;
C.原电池可加快反应速率;
D.酸性越强,结合氢离子的能力越弱.
解答 解:A.电子层越多,离子半径越大;具有相同电子排布的离子,原子序数大的离子半径小,则微粒半径:S2->K+>F-,故A正确;
B.HF分子间含氢键,沸点高,则沸点:HCl<HF,故B正确;
C.原电池可加快反应速率,则反应速率:Fe加入稀H2SO4中<Fe加入稀H2SO4和含少量CuSO4的混合溶液中,故C正确;
D.酸性越强,结合氢离子的能力越弱,则给出质子的能力:CH3COOH<H2O<C2H5OH,故D错误;
故选D.
点评 本题考查元素周期表和周期律的综合应用,为高频考点,把握微粒半径比较、沸点比较及速率比较等为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
5.已知X、Y、Z、R为四种短周期主族元素,其原子序数依次增大,X与Z同主族,其中Y的最外层电子数比次外层电子数少3,下列说法错误的是( )
| A. | 一定条件下X的单质能置换Z的单质 | |
| B. | X、Z、R所形成的离子半径:R>Z>X | |
| C. | Y的单质在R的单质中燃烧可形成白色烟雾 | |
| D. | X和Z的气态氢化物的稳定性:X>Z |
1.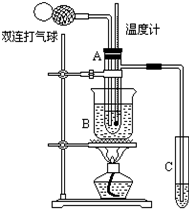 乙醛(CH3CHO)在催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次,反应基本完全.有关物质的沸点见表:
乙醛(CH3CHO)在催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次,反应基本完全.有关物质的沸点见表:
请回答下列问题:
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)2CH3CHO+O2$\frac{\underline{\;\;\;\;\;\;\;CuO\;\;\;\;\;\;\;}}{60℃-80℃}$2CH3COOH.
(2)如图所示,在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在浸入试管A的反应液中;当试管A内的主要反应完成后温度计水银球的位置应在试管A的支管口处.
(3)烧杯B内盛装的液体可以是甘油.
(4)试管C中收集到的是粗产品,若想进一步提纯,可采用的方法是蒸馏;提纯后的产品若在质谱仪中进行测定,其质荷比最大是60(填数值);若在核磁共振仪中进行测定,其核磁共振氢谱共有2种峰,峰面积之比为3:1或1:3.
 乙醛(CH3CHO)在催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次,反应基本完全.有关物质的沸点见表:
乙醛(CH3CHO)在催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次,反应基本完全.有关物质的沸点见表:| 物质 | 乙醛 | 乙酸 | 甘油 | 乙醇 | 水 |
| 沸点/℃ | 20.8 | 117.9 | 290 | 78.2 | 100 |
(1)试管A内在60℃~80℃时发生的主要反应的化学方程式为(注明反应条件)2CH3CHO+O2$\frac{\underline{\;\;\;\;\;\;\;CuO\;\;\;\;\;\;\;}}{60℃-80℃}$2CH3COOH.
(2)如图所示,在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在浸入试管A的反应液中;当试管A内的主要反应完成后温度计水银球的位置应在试管A的支管口处.
(3)烧杯B内盛装的液体可以是甘油.
(4)试管C中收集到的是粗产品,若想进一步提纯,可采用的方法是蒸馏;提纯后的产品若在质谱仪中进行测定,其质荷比最大是60(填数值);若在核磁共振仪中进行测定,其核磁共振氢谱共有2种峰,峰面积之比为3:1或1:3.
18.下列物质中,在一定条件下不能发生水解反应的是( )
| A. | 葡萄糖 | B. | 淀粉 | C. | 蛋白质 | D. | 纤维素 |
15.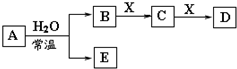 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断错误的是( )
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断错误的是( )
 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断错误的是( )
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去)下列推断错误的是( )| A. | 若X是Na2CO3,C为含极性键的非极性分子,则A一定是氯气,且D和E不反应 | |
| B. | 若A是单质,B和D的反应是OH-+HCO3-═H2O+CO32-,则E是一种清洁的能源 | |
| C. | 若D为CO,C能和E反应,则A一定为Na2O2 | |
| D. | 若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐 |
2.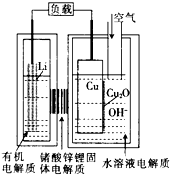 正在研制的一种“高容量、低成本”锂一铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )
正在研制的一种“高容量、低成本”锂一铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )
 正在研制的一种“高容量、低成本”锂一铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )
正在研制的一种“高容量、低成本”锂一铜空气燃料电池.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )| A. | 通空气时,铜被腐蚀,表面产生CuO | |
| B. | 放电一段时间后右侧水溶液电解质中LiOH浓度逐渐增大 | |
| C. | 放电时,正极的电极反应式为Cu2O+H2O+2e-=2Cu+2OH- | |
| D. | 整个反应过程中,铜相当于催化剂 |
19.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 235g的${\;}_{92}^{235}U$发生裂变反应:${\;}_{92}^{235}$U+${\;}_0^1$n$\stackrel{裂变}{→}$${\;}_{38}^{90}$Sr+${\;}_{54}^{136}$U+10${\;}_0^1$n,净产生的中子(${\;}_0^1$n)数为10NA | |
| B. | 12g石墨烯(单层石墨)中含有六元环的个数为NA | |
| C. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| D. | 标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |