题目内容
下列实验操作可以达到实验目的是( )
| 实验目的 | 实验操作 | |
| A. | 验证乙炔能被酸性高锰酸钾溶液氧化 | 将电石与饱和食盐水反应生成的气体通入酸性高锰酸钾溶液,观察溶液是否褪色 |
| B. | 检验淀粉水解产物的还原性 | 取少量淀粉溶液,与稀硫酸共热后再加入银氨溶液,水浴加热,观察是否出现银镜 |
| C. | 除去乙酸乙酯中混有的少量乙酸 | 加入足量饱和Na2CO3溶液,振荡,静置,分液,取出上层液体 |
| D. | 检验溴乙烷中的溴元素 | 取少量溴乙烷,与氢氧化钠溶液共热后加入硝酸银溶液,观察是否出现白色沉淀 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.电石不纯,与水反应生成乙炔的同时也生成硫化氢、磷化氢等;
B.银镜反应应在碱性条件下进行;
C.乙酸乙酯不溶液饱和碳酸钠溶液,而乙酸可与碳酸钠反应;
D.应先酸化后再检验.
B.银镜反应应在碱性条件下进行;
C.乙酸乙酯不溶液饱和碳酸钠溶液,而乙酸可与碳酸钠反应;
D.应先酸化后再检验.
解答:
解:A.电石不纯,与水反应生成乙炔的同时也生成硫化氢、磷化氢等,都可与高锰酸钾溶液反应,应先除杂,故A错误;
B.银镜反应应在碱性条件下进行,题中没有加入碱调节溶液pH,故B错误;
C.乙酸和碳酸钠反应生成可溶性的乙酸钠,乙酸乙酯和碳酸钠不反应且乙酸乙酯不溶于水,然后采用分液的方法分离,所以能实现实验目的,故C正确;
D.溴乙烷在碱性条件下水解生成溴离子,应先酸化后再检验,否则生成AgOH沉淀而影响实验结果,故D错误.
故选C.
B.银镜反应应在碱性条件下进行,题中没有加入碱调节溶液pH,故B错误;
C.乙酸和碳酸钠反应生成可溶性的乙酸钠,乙酸乙酯和碳酸钠不反应且乙酸乙酯不溶于水,然后采用分液的方法分离,所以能实现实验目的,故C正确;
D.溴乙烷在碱性条件下水解生成溴离子,应先酸化后再检验,否则生成AgOH沉淀而影响实验结果,故D错误.
故选C.
点评:本题考查了实验方案的评价,为高频考点,侧重于学生的分析能力和实验能力的考查,涉及物质的分离和提纯、物质的检验等知识点,根据物质的性质确定除杂剂,再结合物质反应条件来分析解答,易错选项是AD,注意:银镜反应及醛、新制Cu(OH)2悬浊液反应都必须在碱性条件下,为易错点.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
下列说法正确的是( )
| A、强电解质溶液一定比弱电解质溶液的导电性强 |
| B、强电解质的水溶液中不存在电解质分子 |
| C、强电解质都是离子化合物,弱电解质都是共价化合物 |
| D、不同的弱电解质只要物质的量浓度相同,电离程度也就相同 |
对配合物[Cu(NH3)4]SO4的叙述,错误的是( )
| A、Cu2+和NH3之间以配位键结合 | ||
B、[Cu(NH3)4]2+和SO
| ||
| C、Cu2+和NH3之间以离子键结合 | ||
D、[Cu(NH3)4]SO4在水中全部电离成[Cu(NH3)4]2+和SO
|
物质的量浓度相同的下列各溶液①NaHSO4 ②NaHCO3 ③Na2CO3 ④Na2SO4,由水电离出的氢氧根浓度由大到小的顺序( )
| A、④③②① | B、①②③④ |
| C、③②④① | D、③④②① |
下列叙述正确的是( )
| A、原子晶体中各相邻原子之间都以共价键结合 |
| B、分子晶体中都存在范德瓦耳斯力,分子内都存在共价键 |
| C、HF、HCl、HBr、HI四种物质的沸点依次升高 |
| D、干冰和氯化铵分别受热变为气体所克服的粒子间相互作用属于同种类型 |
下列试剂加入少量溴水充分振荡后,上层几乎无色的是( )
| A、己烷 | B、溴苯 | C、乙醇 | D、甲苯 |
下列化学用语的书写,正确的是( )
A、氮气的电子式: |
B、硫原子的结构示意图: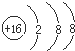 |
C、溴化钠的电子式: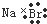 |
| D、CO2分子的结构式:O=C=O |
下列关于盐类水解反应的应用说法正确的是( )
| A、可以把FeCl3固体直接溶于水制FeCl3溶液 |
| B、热的纯碱溶液去油污效果好 |
| C、加热AlCl3溶液可得到AlCl3固体 |
| D、Mg粉投入到饱和NH4Cl溶液中无明显现象 |