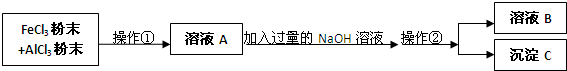题目内容
2.请写出除去下列杂质的化学方程式.| 物质 | 杂质 | 化学方程式 | |
| ① | Na2CO3溶液 | NaHCO3 | NaOH+NaHCO3=H2O+Na2CO3 |
| ② | Mg粉 | Al 粉 | 2Al+2H2O+2NaOH=2NaAlO2+3H2↑ |
| ③ | CO2 | SO2 | SO2+2NaHCO3═Na2SO3+H2O+2CO2 |
分析 ①碳酸氢钠与NaOH反应生成碳酸钠;
②Al与NaOH溶液反应,而Mg不能;
③二氧化硫与碳酸氢钠反应生成亚硫酸钠、水、二氧化碳.
解答 解:①碳酸氢钠与NaOH反应生成碳酸钠,发生的反应为NaOH+NaHCO3=H2O+Na2CO3,故答案为:NaOH+NaHCO3=H2O+Na2CO3;
②Al与NaOH溶液反应,而Mg不能,发生的反应为2Al+2H2O+2NaOH=2NaAlO2+3H2↑,故答案为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑;
③二氧化硫与碳酸氢钠反应生成亚硫酸钠、水、二氧化碳,发生的反应为SO2+2NaHCO3═Na2SO3+H2O+2CO2,故答案为:SO2+2NaHCO3═Na2SO3+H2O+2CO2.
点评 本题考查化学反应方程式的书写及混合物分离提纯,为高频考点,把握物质的性质、性质差异及发生的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.下列检验Cl-的方法正确的是( )
| A. | 在某溶液中滴加AgNO3溶液,若产生白色沉淀,说明该溶液中有Cl- | |
| B. | 在某溶液中先滴加盐酸,再滴加AgNO3溶液,若产生白色沉淀,说明溶液中有Cl- | |
| C. | 在某溶液中先滴加AgNO3溶液,产生色沉淀,再滴加盐酸,沉淀不消失,说明溶液中Cl- | |
| D. | 某溶中滴加用HNO3酸化的AgNO3溶液,若产生白色沉淀,说明溶液中有Cl- |
13.含有非极性键的离子化合物是( )
| A. | NH4Cl | B. | NaOH | C. | Na2O2 | D. | MgCl2 |
17.某有机物X的结构简式如图所示,则下列有关说法中正确的是( )


| A. | 有机物X的分子式为Cl2H15O | |
| B. | X分子不能使酸性高锰酸钾溶液褪色 | |
| C. | X分子中一定在同一个平面内的碳原子最多6个 | |
| D. | 在Ni作催化剂的条件下,1molX最多能与4molH2加成 |
7.下列有关的叙述正确的是( )
| A. | HClO是弱酸,所以NaClO是弱电解质 | |
| B. | 固体的NaCl不导电,熔融态的NaCl可以导电 | |
| C. | 根据分散质粒子的直径大小,分散系可分为溶液、浊液和胶体,浊液的分散质粒子大小介于溶液与胶体之间 | |
| D. | “血液透析”原理与胶体的性质无关 |
14.以MnO2为原料制得的MnCl2溶液中常含有Cu2+、Pb2+、Cd2+等金属离子,通过添加过量难溶电解质MnS,可使这些金属离子形成硫化物沉淀,经过滤除去包括MnS在内的沉淀,再经蒸发、结晶,可得纯净的MnCl2.根据上述实验事实,可推知MnS具有的相关性质是( )
| A. | 具有吸附性 | |
| B. | 溶解度大于CuS、PbS、CdS | |
| C. | 溶解度小于CuS、PbS、CdS | |
| D. | MnO2的氧化性强于Cu2+、Pb2+、Cd2+等金属离子 |
12.下列解释事实的化学方程式不正确的是( )
| A. | 将氯气与通入冷的消石灰中反应制漂白粉:2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O | |
| B. | 向较浓的Na2SiO3溶液中滴加适量盐酸制得硅酸胶体:Na2SiO3+2HCl═2NaCl+H2SiO3(胶体) | |
| C. | 铁在潮湿的环境中生锈:3Fe+4H2O═Fe3O4+4H2↑ | |
| D. | 用氢氟酸刻蚀玻璃:SiO2+4HF═SiF4+2H2O |
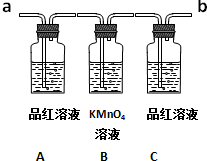 已知二氧化硫可使高锰酸钾溶液褪色,反应的化学方程式为:5SO2+2KMnO4+2H2O═K2SO4+2MnSO4+2H2SO4用如图装置来验证浓硫酸与木炭在加热条件下反应的产物中含有SO2和CO2
已知二氧化硫可使高锰酸钾溶液褪色,反应的化学方程式为:5SO2+2KMnO4+2H2O═K2SO4+2MnSO4+2H2SO4用如图装置来验证浓硫酸与木炭在加热条件下反应的产物中含有SO2和CO2