题目内容
14.下列说法正确的是( )| A. | 加热法可以除去氯化铵中的少量碘单质 | |
| B. | 向试液中滴加双氧水可KSCN溶液,溶液变为红色,则试液中一定含Fe2+ | |
| C. | 向某固体中滴加稀硫酸,产生的气体能使澄清石灰水变浑浊,则该固体一定是苏打或小苏打 | |
| D. | 向含少量硫酸铁的硫酸铜溶液中加入过量的氧化铜,过滤,得到纯净硫酸铜溶液 |
分析 A.氯化铵加热分解,不能通过加热的方法除去碘单质;
B.加入顺序错误,应该先滴加硫氰化钾溶液,然后再加入双氧水;
C.生成的气体可能为二氧化硫,该固体可能为亚硫酸钠和亚硫酸氢钠;
D.加入氧化铜后,铁离子能够转化成氢氧化铁沉淀.
解答 解:A.碘单质能够升华,但是氯化铵加热会分解,所以不能用加热法法除去氯化铵中的少量碘单质,故A错误;
B.检验亚铁离子时,应该先向试液中滴加KSCN溶液,溶液没有明显现象,然后再加入双氧水,若溶液变为红色,则试液中一定含Fe2+,故B错误;
C.向某固体中滴加稀硫酸,产生的气休能使澄清石灰水变浑浊,生成的气体可能为二氧化硫,则该固体可能为亚硫酸钠或亚硫酸氢钠,不一定为碳酸钠或碳酸氢钠,故C错误;
D.铁离子只能存在于酸性溶液中,则向含少量硫酸铁的硫酸铜溶液中加入过量的氧化铜会生成氢氧化铁沉淀和硫酸铜,过滤后得到纯净硫酸铜溶液,故D正确;
故选D.
点评 本题考查性质实验方案的设计,侧重考查物质的分离与提纯方法、常见离子的检验方法,题目难度中等,注意掌握常见物质分离与提纯方法,明确常见离子的性质及检验方法.

练习册系列答案
相关题目
5.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 电解精炼铜的过程中,镁转移NA个电子时,阳极溶解铜的质量为32g | |
| B. | 1molNa2O2固体中含离子总数为4NA | |
| C. | 1mol羟基与17g NH3所含电子数之比为9:10 | |
| D. | 1molNa2CO3晶体中含阴离子数小于1NA |
2.铬及其化合物在工业上有许多用途,但化工废料铬渣对人体健康有很大危害,以制革工也产生的含铬污泥为原料,回收污泥中三价铬的工艺流程图如图所示(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+)
:
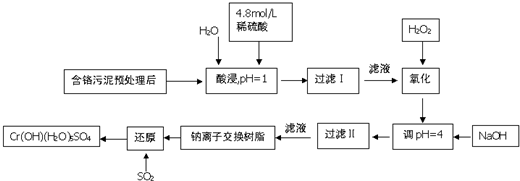
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
回答下列问题:
(1)能提高浸取时三价铬的浸取率的措施有ABC(填字母)
A.将含铬污泥粉碎并适当延长浸取时间
B.升高温度并不断搅拌
C.多次浸取,合并浸取液
D.缩短浸取时间
(2)氧化过程中加入H2O2,除了把Cr3+氧化为Cr2O72-外,另一个作用时2Fe2++H2O2+2H+=2Fe3++2H2O(用离子方程式表示).
(3)过滤Ⅱ产生的沉淀是Fe(OH)3(填化学式).
(4)钠离子交换树脂的原理为:Mn++nNaR═MRn+nNa+,被交换的杂质离子是Al3+、Ca2+、Mg2+(填离子符号).
(5)每生成1molCr(OH)(H2O)5SO4,消耗SO2物的质量为1.5mol.
(6)工业上可用电解法处理含Cr2O72-的酸性废水,具体方法是将含Cr2O72-的酸性废水放入电解槽内,加入适量的NaCl,以铁和石墨为电极进行电解.经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去.
①铁电极与直流电源正极(填“正极”或“负极”)相连,加入适量NaCl的目的是增大溶液导电能力;
②若电解后的溶液中c(Fe3+)为2.0×10-13mol•L-1,则溶液中c(Cr3+)为3.0×10-6mol/L(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp=[Cr(OH)3]=6.0×10-31)
:

常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.0 | - | - | - |
| 沉淀完全是的pH | 3.7 | 9.0 | 11.1 | 8 | 9(>9溶解) |
(1)能提高浸取时三价铬的浸取率的措施有ABC(填字母)
A.将含铬污泥粉碎并适当延长浸取时间
B.升高温度并不断搅拌
C.多次浸取,合并浸取液
D.缩短浸取时间
(2)氧化过程中加入H2O2,除了把Cr3+氧化为Cr2O72-外,另一个作用时2Fe2++H2O2+2H+=2Fe3++2H2O(用离子方程式表示).
(3)过滤Ⅱ产生的沉淀是Fe(OH)3(填化学式).
(4)钠离子交换树脂的原理为:Mn++nNaR═MRn+nNa+,被交换的杂质离子是Al3+、Ca2+、Mg2+(填离子符号).
(5)每生成1molCr(OH)(H2O)5SO4,消耗SO2物的质量为1.5mol.
(6)工业上可用电解法处理含Cr2O72-的酸性废水,具体方法是将含Cr2O72-的酸性废水放入电解槽内,加入适量的NaCl,以铁和石墨为电极进行电解.经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去.
①铁电极与直流电源正极(填“正极”或“负极”)相连,加入适量NaCl的目的是增大溶液导电能力;
②若电解后的溶液中c(Fe3+)为2.0×10-13mol•L-1,则溶液中c(Cr3+)为3.0×10-6mol/L(已知Ksp[Fe(OH)3]=4.0×10-38,Ksp=[Cr(OH)3]=6.0×10-31)
9.下列电子式书写不正确的是( )
| A. | 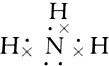 | B. | 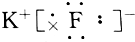 | C. | 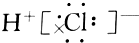 | D. | 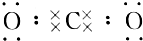 |
19.下列化合物结构中有两种常见官能团的是( )
| A. | HOCH2CH2Cl | B. | CH3CH2OH | C. | CH3COOH | D. | 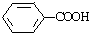 |
6.下列关于铷(Rb)的叙述中,正确的是( )
| A. | 铷的密度比钠小,熔点比钠高 | |
| B. | 铷与冷水不反应,但与热水反应,并放出氢气 | |
| C. | 铷盐大多数易溶于水 | |
| D. | 铷的原子半径和离子半径都比钠小 |
4.下列关于铜电极的叙述中,正确的是( )
| A. | 电解稀硫酸制H2、O2时铜作阳极 | B. | 用电解法精炼粗铜时粗铜作阴极 | ||
| C. | 在镀件上电镀铜时用金属铜作阴极 | D. | 铜锌原电池中铜是正极 |
5.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
| A. | 冰醋酸、纯碱、芒硝、生石灰分别属于酸、碱、盐、氧化物 | |
| B. | HClO、H2SO4(浓)、HNO3均具有强氧化性,都是氧化性酸 | |
| C. | 漂白粉、福尔马林、冰水、王水、氯水均为混合物 | |
| D. | Na2O、NaOH、Na2CO3、NaCl都属于钠的含氧化合物 |