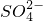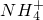题目内容
根据下列化学实验事实得出的结论一定正确的是( )
分析:A、能和氯化钡反应生成白色沉淀不溶于盐酸的离子可能是银离子也可能是硫酸根离子;
B、能使湿润的红色石蕊试纸变蓝的气体应该显碱性,气体中只有氨气显碱性;
C、铝和氢氧化钠溶液反应,镁和氢氧化钠溶液不反应;
D、醛类物质和氢氧化铜悬浊液发生反应的条件必须是在碱性环境下才能发生.
B、能使湿润的红色石蕊试纸变蓝的气体应该显碱性,气体中只有氨气显碱性;
C、铝和氢氧化钠溶液反应,镁和氢氧化钠溶液不反应;
D、醛类物质和氢氧化铜悬浊液发生反应的条件必须是在碱性环境下才能发生.
解答:解:A、能和氯化钡反应生成不溶于盐酸的白色沉淀的离子可能是硫酸根离子也可能是银离子,所以该溶液中不一定含有硫酸根离子,故A错误;
B、能使湿润的红色石蕊试纸变蓝色的气体只有氨气,所以向某无色溶液中加入氢氧化钠溶液并加热产生氨气,说明原溶液中含有铵根离子,故B正确;
C、铝具有两性,能和强碱反应生成可溶性的盐,镁和氢氧化钠不反应,所以不能用过量烧碱溶液除去铝粉中混有的少量镁粉,但可以用过量氢氧化钠溶液除去镁粉中的铝粉,故C错误;
D、该题中硫酸铜过量导致溶液呈酸性,醛类物质和氢氧化铜悬浊液发生反应的条件必须是在碱性环境下才能发生,所以不会看到红色沉淀,故D错误.
故选B.
B、能使湿润的红色石蕊试纸变蓝色的气体只有氨气,所以向某无色溶液中加入氢氧化钠溶液并加热产生氨气,说明原溶液中含有铵根离子,故B正确;
C、铝具有两性,能和强碱反应生成可溶性的盐,镁和氢氧化钠不反应,所以不能用过量烧碱溶液除去铝粉中混有的少量镁粉,但可以用过量氢氧化钠溶液除去镁粉中的铝粉,故C错误;
D、该题中硫酸铜过量导致溶液呈酸性,醛类物质和氢氧化铜悬浊液发生反应的条件必须是在碱性环境下才能发生,所以不会看到红色沉淀,故D错误.
故选B.
点评:本题考查了离子、醛基的检验和元素化合物的性质等知识点,根据物质的性质来分析解答即可,难度不大,注意醛类物质和氢氧化铜悬浊液发生反应的条件必须是在碱性环境下才能发生,为易错点.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
根据下列化学实验事实得出的结论一定正确的是( )
| A、向某无色溶液中先加入氯化钡溶液,生成白色沉淀,再加入足量盐酸,沉淀不溶解. 结论:该溶液中一定有SO42- | B、用洁净的铂丝沾取某无色溶液在酒精灯上灼烧,透过蓝色钴玻璃火焰呈紫色 结论:该溶液中一定有K+ | C、向某无色溶液中加稀盐酸,产生无色无味且能使澄清石灰水变混浊的气体 结论:溶液中一定有CO32- | D、用一束光照射Fe(OH)3胶体和FeCl3溶液,光束通过Fe(OH)3胶体时可看见一条光亮的“通路”, 结论:丁达尔效应可鉴别胶体和溶液 |