题目内容
I. 下列实验操作或对实验事实的叙述中,正确的在横线里打√,错误的在横线里打×:
( )(1)实验室制取乙烯时,必须将温度计的水银球插入反应液液面以下,根据温度计指示的温度来调节酒精灯火焰大小,以控制反应液的温度.
( )(2)在洁净的试管里加入1mL2%的氨水,然后一边摇动试管,一边逐滴滴入2%的硝酸银溶液,至最初产生的沉淀恰好溶解为止,即得银氨溶液.
( )(3)用稀硝酸清洗做过银镜反应实验的试管.
( )(4)实验室制肥皂时,将适量植物油和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,即可得到肥皂.
( )(5)进行纤维素水解实验时,把一小团蓬松脱脂棉放入试管,滴入少量浓硫酸搅拌,使脱脂棉变成糊状,再加入一定量的水,加热至溶液呈亮棕色,然后加入新制的Cu(OH)2加热至沸腾即可.
II.现安装一套实验室利用液一液反应制备气体的装置,有人设计了五步操作,请你安排出正确而简捷的程序,将序号(1、2、3…)填入括号内.
( )将蒸馏烧瓶固定在铁架台上.
( )把酒精灯放在铁架台上,根据酒精灯确定铁圈的高度,固定铁圈,放好石棉网.
( )用漏斗向蒸馏烧瓶中加入一种液体反应物,再向分液漏斗中加入另一种液体反应物,并将导气管放入气体收集器中.
( )检查装置的气密性(利用对固定装置进行微热的方法来检查气密性,假定瓶口漏气而需要更换橡皮塞).
( )在蒸馏烧瓶上装好分液漏斗,连接好导气管.
III.某校学生小组为探究乙酸、碳酸和苯酚的酸性强弱,进行下述实验.
该校学生设计了如图的实验装置(夹持仪器已略去).
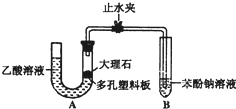
(1)某生检查装置A的气密性时,先关闭止水夹,从左管向U型管内加水,至左管液面高于右管液面,静置一段时间后,若U型管两侧液面差不发生变化,则气密性良好.你认为该生的操作正确与否? (填“正确”或“错误”)
大理石与乙酸溶液反应的化学方程式为
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为
反应的离子方程式为
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,理由是乙酸有挥发性,挥发出的乙酸也可以和苯酚钠溶液反应,生成苯酚.改进该装置的方法是 .
(
(
(
(
(
II.现安装一套实验室利用液一液反应制备气体的装置,有人设计了五步操作,请你安排出正确而简捷的程序,将序号(1、2、3…)填入括号内.
(
(
(
(
(
III.某校学生小组为探究乙酸、碳酸和苯酚的酸性强弱,进行下述实验.
该校学生设计了如图的实验装置(夹持仪器已略去).

(1)某生检查装置A的气密性时,先关闭止水夹,从左管向U型管内加水,至左管液面高于右管液面,静置一段时间后,若U型管两侧液面差不发生变化,则气密性良好.你认为该生的操作正确与否?
大理石与乙酸溶液反应的化学方程式为
(2)装置A中反应产生的气体通入苯酚钠溶液中,实验现象为
反应的离子方程式为
(3)有学生认为(2)中的实验现象不足以证明碳酸的酸性比苯酚强,理由是乙酸有挥发性,挥发出的乙酸也可以和苯酚钠溶液反应,生成苯酚.改进该装置的方法是
考点:性质实验方案的设计,化学实验方案的评价
专题:实验评价题
分析:Ⅰ、(1)制取乙烯在170℃,需测定反应液的温度;
(2)向硝酸银溶液中滴加氨水,制取银氨溶液;
(3)Ag能与硝酸反应;
(4)植物油和NaOH溶液混合发生水解生成高级脂肪酸盐,需加饱和食盐水发生盐析;
(5)纤维素水解后溶液显酸性,而检验水解产物葡萄糖,应在碱性溶液中.
Ⅱ、实验室利用液一液反应制备气体的装置时,根据先下后上和先检验装置气密性后加入药品的原则组装仪器,据此进行解答.
Ⅲ、(1)根据体系内产生的压强是否变化来判断装置的气密性,碳酸钙和醋酸反应生成醋酸钙和水、二氧化碳;
(2)二氧化碳和苯酚钠反应生成不易溶于水的苯酚和碳酸氢钠,根据离子方程式的书写规则书写;
(3)要防止醋酸干扰实验,在气态未和苯酚反应前将其除去,可选用饱和的碳酸氢钠溶液除去醋酸且又不引进新的杂质气体.
(2)向硝酸银溶液中滴加氨水,制取银氨溶液;
(3)Ag能与硝酸反应;
(4)植物油和NaOH溶液混合发生水解生成高级脂肪酸盐,需加饱和食盐水发生盐析;
(5)纤维素水解后溶液显酸性,而检验水解产物葡萄糖,应在碱性溶液中.
Ⅱ、实验室利用液一液反应制备气体的装置时,根据先下后上和先检验装置气密性后加入药品的原则组装仪器,据此进行解答.
Ⅲ、(1)根据体系内产生的压强是否变化来判断装置的气密性,碳酸钙和醋酸反应生成醋酸钙和水、二氧化碳;
(2)二氧化碳和苯酚钠反应生成不易溶于水的苯酚和碳酸氢钠,根据离子方程式的书写规则书写;
(3)要防止醋酸干扰实验,在气态未和苯酚反应前将其除去,可选用饱和的碳酸氢钠溶液除去醋酸且又不引进新的杂质气体.
解答:
解:Ⅰ、(1)制取乙烯时在170℃,需测定反应液的温度,必须将温度计的水银球插入反应液液面以下,根据温度计指示的温度来调节酒精灯火焰大小,以控制反应液的温度,故答案为:√;
(2)向硝酸银溶液中滴加氨水,生成白色沉淀,继续滴加氨水,至生成的沉淀恰好溶解,所得溶液为银氨溶液,故答案为:×;
(3)因Ag能互硝酸反应,而溶解,则可用稀硝酸清洗做过银镜反应实验的试管,故答案为:√;
(4)实验室制肥皂时,将适量植物油和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,然后加饱和食盐水发生盐析,即可得到肥皂,故答案为:×;
(5)进行纤维素水解实验时,把一小团蓬松脱脂棉放入试管,滴入少量浓硫酸搅拌,使脱脂棉变成糊状,再加入一定量的水,加热至溶液呈亮棕色,然后先加碱至碱性,再加入新制的Cu(OH)2加热至沸腾来检验水解产物,故答案为:×;
Ⅱ、在安装利用液一液反应制备气体的装置时,应该按照先下后上和先检验装置气密性后加入药品的原则组装仪器,即:先根据酒精灯高度确定铁圈高度,然后
将蒸馏烧瓶固定在铁架台上,接着再将蒸馏烧瓶上装好分液漏斗,连接好导气管,这样装置连接完毕,下一步需要检查装置气密性,最后放入药品,
故答案为:2;1;5;4;3.
Ⅲ、(1)U型管两侧液面差能产生压强,所以能判断装置的气密性,故正确;碳酸钙和醋酸反应生成醋酸钙和水、二氧化碳,反应方程式为CaCO3+2CH3COOH=Ca(CH3COO)2+CO2↑+H2O,
故答案为:正确;CaCO3+2CH3COOH=Ca(CH3COO)2+CO2↑+H2O;
(2)二氧化碳和苯酚钠反应生成不易溶于水的苯酚和碳酸氢钠,所以看到的现象是溶液出现浑浊,反应离子方程式为:C6H5O-+CO2+H2O→C6H5OH+HCO3-,
故答案为:溶液出现浑浊;C6H5O-+CO2+H2O→C6H5OH+HCO3-;
(3)要防止醋酸干扰实验,在气态未和苯酚反应前将其除去,可选用饱和的碳酸氢钠溶液除去醋酸且又不引进新的杂质气体,所以在装置A和B之间连一个盛有饱和碳酸氢钠溶液的洗气瓶除去醋酸,
故答案为:在装置A和B之间连一个盛有饱和碳酸氢钠溶液的洗气瓶.
(2)向硝酸银溶液中滴加氨水,生成白色沉淀,继续滴加氨水,至生成的沉淀恰好溶解,所得溶液为银氨溶液,故答案为:×;
(3)因Ag能互硝酸反应,而溶解,则可用稀硝酸清洗做过银镜反应实验的试管,故答案为:√;
(4)实验室制肥皂时,将适量植物油和NaOH溶液混合,并不断搅拌、加热,直到混合物变稠,然后加饱和食盐水发生盐析,即可得到肥皂,故答案为:×;
(5)进行纤维素水解实验时,把一小团蓬松脱脂棉放入试管,滴入少量浓硫酸搅拌,使脱脂棉变成糊状,再加入一定量的水,加热至溶液呈亮棕色,然后先加碱至碱性,再加入新制的Cu(OH)2加热至沸腾来检验水解产物,故答案为:×;
Ⅱ、在安装利用液一液反应制备气体的装置时,应该按照先下后上和先检验装置气密性后加入药品的原则组装仪器,即:先根据酒精灯高度确定铁圈高度,然后
将蒸馏烧瓶固定在铁架台上,接着再将蒸馏烧瓶上装好分液漏斗,连接好导气管,这样装置连接完毕,下一步需要检查装置气密性,最后放入药品,
故答案为:2;1;5;4;3.
Ⅲ、(1)U型管两侧液面差能产生压强,所以能判断装置的气密性,故正确;碳酸钙和醋酸反应生成醋酸钙和水、二氧化碳,反应方程式为CaCO3+2CH3COOH=Ca(CH3COO)2+CO2↑+H2O,
故答案为:正确;CaCO3+2CH3COOH=Ca(CH3COO)2+CO2↑+H2O;
(2)二氧化碳和苯酚钠反应生成不易溶于水的苯酚和碳酸氢钠,所以看到的现象是溶液出现浑浊,反应离子方程式为:C6H5O-+CO2+H2O→C6H5OH+HCO3-,
故答案为:溶液出现浑浊;C6H5O-+CO2+H2O→C6H5OH+HCO3-;
(3)要防止醋酸干扰实验,在气态未和苯酚反应前将其除去,可选用饱和的碳酸氢钠溶液除去醋酸且又不引进新的杂质气体,所以在装置A和B之间连一个盛有饱和碳酸氢钠溶液的洗气瓶除去醋酸,
故答案为:在装置A和B之间连一个盛有饱和碳酸氢钠溶液的洗气瓶.
点评:本题考查了化学实验方案的评价及其化学实验操作的先后顺序,涉及乙烯的制备、银氨溶液的制备、肥皂的制备及水解产物的检验实验等,难度不大,注意苯酚钠溶液和二氧化碳反应生成碳酸氢钠而不是碳酸钠,为易错点.

练习册系列答案
相关题目
下列溶液中的氯离子数目与50mL 1mol?L-1的FeCl3溶液中氯离子数目相等的是( )
| A、150 mL 1 mol?L-1的NaCl |
| B、75 mL 2 mol?L-1的NH4Cl |
| C、150 mL 3 mol?L-1的KCl |
| D、75 mL 2 mol?L-1的CaCl2 |
下列的离子方程式书写不正确的是( )
| A、硫酸与氯化钡反应:SO42-+Ba2+=BaSO4↓ |
| B、碳酸钙放入稀盐酸中:CO32-+2H+=CO2↑+H2O |
| C、稀硫酸滴在锌片上:Zn+2H+=Zn2++H2↑ |
| D、CuO和盐酸反应:CuO+2H+=Cu2++H2O |
常温下,下列各溶液中微粒的物质的量浓度关系正确的是( )
| A、0.1 mol?L-1的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| B、NaA溶液的pH=8,c(Na+)-c(A-)=9.9×10-7 mol?L-1 |
| C、将0.1mol/L的Na2S溶液与0.1mol/L的NaHS溶液等体积混合,所得溶液中:c(OH-)=c(H+)+c(S2-)+2c(HS-)+3c(H2S) |
| D、将25mL0.2mol/L的盐酸与100mL0.1mol/L的氨水混合,所得溶液中:c(Cl-)>c(NH4+)>c(NH3?H2O)>c(OH-)>c(H+) |
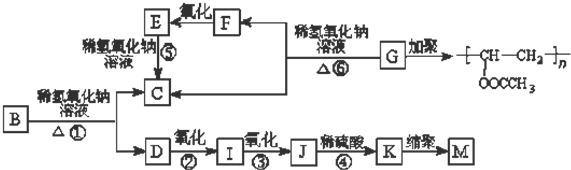

 表示(其中X、Y均不为氢):写出符合上述通式且能发生银镜反应的四种物质的结构简式
表示(其中X、Y均不为氢):写出符合上述通式且能发生银镜反应的四种物质的结构简式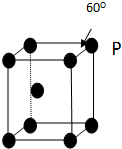 A、B、C、D、E五种元素其核电荷数依次增大.A原子只有1个s电子,B原子L层中s电子和p电子数目相同,B、C、D属于同周期且相邻,E原子内层均饱和,N层上只有两个电子.
A、B、C、D、E五种元素其核电荷数依次增大.A原子只有1个s电子,B原子L层中s电子和p电子数目相同,B、C、D属于同周期且相邻,E原子内层均饱和,N层上只有两个电子.