题目内容
已知砒霜As2O3与Zn可以发生如下反应:
As2O3+ Zn+ H2SO4- AsH3+ ZnSO4+ H2O
(1)请配平该方程式并用双线桥法标出电子转移的方向和数目:
.
(2)As2O3在上述反应中显示的性质是 .
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化剂是 ,还原产物是 .
(4)若生成0.1mol AsH3,则转移的电子数为 .
(1)请配平该方程式并用双线桥法标出电子转移的方向和数目:
(2)As2O3在上述反应中显示的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)该反应的氧化剂是
(4)若生成0.1mol AsH3,则转移的电子数为
考点:氧化还原反应方程式的配平,氧化还原反应
专题:氧化还原反应专题
分析:每个Zn原子失去2个电子,2个As原子得到12个电子,根据电子守恒,转移电子是12,得到配平的方程式,As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O中,As元素的化合价降低,则As2O3为氧化剂,被还原,还原产物为AsH3;Zn元素的化合价升高,Zn元素被氧化,则ZnSO4为氧化产物,以此来解答.
解答:
解:(1)反应中,每个Zn原子失去2个电子,2个As原子得到12个电子,根据电子守恒,转移电子是12,所以Zn的前边系数是6,AsH3的系数是2,根据元素守恒,得到配平后的方程式为:As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O,则双线桥法标出电子转移的方向和数目为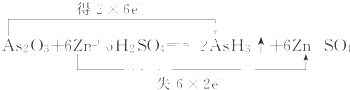 ,故答案为:
,故答案为: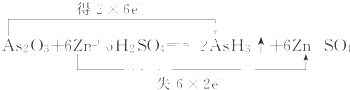 ;
;
(2)As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O中,As元素的化合价降低,则As2O3为氧化剂,表现氧化性,故答案为:A;
(3)As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O中中,As元素的化合价降低,则As2O3为氧化剂,被还原,还原产物为AsH3;故答案为:As2O3;AsH3;
(4)As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O中生成2molAsH3转移12mol电子,则生成0.1molAsH3,则转移的电子数为0.6mol电子,即转移的电子数为0.6NA,
故答案为:0.6NA.
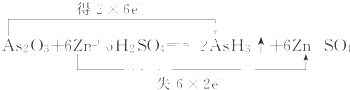 ,故答案为:
,故答案为: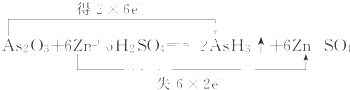 ;
;(2)As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O中,As元素的化合价降低,则As2O3为氧化剂,表现氧化性,故答案为:A;
(3)As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O中中,As元素的化合价降低,则As2O3为氧化剂,被还原,还原产物为AsH3;故答案为:As2O3;AsH3;
(4)As2O3+6Zn+6H2SO4═2AsH3↑+6ZnSO4+3H2O中生成2molAsH3转移12mol电子,则生成0.1molAsH3,则转移的电子数为0.6mol电子,即转移的电子数为0.6NA,
故答案为:0.6NA.
点评:本题考查氧化还原反应及计算,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度中等.

练习册系列答案
相关题目
反应A(g)+3B(g)?2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
| A、v(A)=0.15 mol/(L?min) |
| B、v(B)=0.06 mol/(L?min) |
| C、v(C)=0.04 mol/(L?s) |
| D、v(D)=0.01 mol/(L?s)) |
一个原电池的总反应的离子方程式是Zn+Cu2+═Zn2++Cu,该原电池的合理组成是( )
| 正极 | 负极 | 电解质溶液 | |
| A | Cu | Zn | CuSO4 |
| B | Cu | Zn | H2SO4 |
| C | Zn | Cu | CuCl2 |
| D | Mg | Zn | CuCl2 |
| A、A | B、B | C、C | D、D |
已知反应FeO(s)+C(s)=CO(g)+Fe(s)的△H>0,(假设△H,△S不随温度变化而变化),下列叙述中正确的是( )
| A、低温下为自发过程,高温下为非自发过程 |
| B、高温下为自发过程,低温下为非自发过程 |
| C、任何温度下为非自发过程 |
| D、任何温度下为自发过程 |
下列对化学反应速率的认识正确的是( )
| A、H+和OH-的反应活化能接近于零,反应几乎在瞬间完成 |
| B、对于任何化学反应来说,反应速率越大,反应现象就越明显 |
| C、选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大 |
| D、化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加 |
下列分子中既有σ键又有π键的是( )
| A、Cl2 |
| B、HCl |
| C、H2O |
| D、N2 |
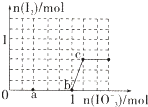 已知含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,则下列判断不正确的是( )
已知含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如图所示,则下列判断不正确的是( )| A、还原性:HSO3->I-,氧化性:IO3->I2>SO42- |
| B、a点处的氧化产物是SO42-,还原产物是I- |
| C、当溶液中的I-为0.4mol时,加入的KIO3一定为0.4mol |
| D、若向KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为:2IO3-+5HSO3-=I2,+5SO42-+3H++H2O |
下列电离方程式书写正确的是( )
| A、H2CO3=2 H++CO32- |
| B、Ca(OH)2=Ca2++(OH)2- |
| C、K2SO4═2K++SO4-2 |
| D、NaHCO3=Na++HCO3- |
 如图是给病人输液用的氯化钠注射溶液的标签.(友情提示:若要用到溶液密度,可用水的密度进行计算)
如图是给病人输液用的氯化钠注射溶液的标签.(友情提示:若要用到溶液密度,可用水的密度进行计算)