题目内容
16.(1)钠、镁、铝均为0.2mol分别与200mL浓度为1mol/L的HCl溶液反应,产生氢气量相等.(2)钠、镁、铝均为0.2mol分别与500mL浓度为1mol/L的HCl溶液反应,产生氢气的体积比为2:4:5.
分析 (1)由于Na能与水反应生成氢气,而Mg、Al不能与水反应,只有HCl反应,故与盐酸反应时,Na一定完全反应,根据2Na~H2↑计算生成氢气物质的量,再根据H原子守恒计算HCl物质的量,根据V=$\frac{n}{c}$需要盐酸的体积;
(2)金属均为0.2mol,n(HCl)=0.5L×0.2mol/L=0.1mol,由2Na~2HCl~H2,2Mg~4HCl~2H2,2Al~6HCl~3H2计算,钠与盐酸的反应中,以Na的物质的量计算.
解答 解:(1)由于Na能与水反应生成氢气,而Mg、Al不能与水反应,只有HCl反应,故与盐酸反应时,Na一定完全反应,根据2Na~H2↑可知,生成氢气物质的量为0.2mol×$\frac{1}{2}$=0.1mol,再根据H原子守恒,可知HCl物质的量为0.1mol×2=0.2mol,故需要盐酸的体积为$\frac{0.2mol}{1mol/L}$=0.2L=200mL,
故答案为:200;
(2)金属均为0.2mol,n(HCl)=0.5L×1mol/L=0.5mol,则
2Na~2HCl~H2,
0.2 0.1
2Mg~4HCl~2H2,
0.2 0.5 0.2
2Al~6HCl~3H2,
0.5 0.25
则生成氢气的质量比等于物质的量之比,均为0.1mol:0.2mol:0.25mol=2:4:5,故答案为:2:4:5.
点评 本题考查化学方程式有关计算,难度不大,涉及过量计算问题,关键是明确Na能与水反应.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
4.下列叙述不正确的是( )
| A. | 牺牲阳极的阴极保护法利用的是原电池原理 | |
| B. | Fe2+能与[Fe(CN)6]3-反应生成带有特征蓝色的沉淀 | |
| C. | 电解质溶液的导电过程一定是电解质溶液的电解过程 | |
| D. | 如果在1.0L Na2CO3溶液中溶解0.010mol的BaSO4,则Na2CO3溶液的最初浓度不得低于0.24 mol/L[已知Ksp(BaSO4)=1.1×10-10; Ksp(BaCO3)=2.6×10-9] |
11.以NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 0.1 mol Cl2溶于水,转移的电子数目为0.1NA | |
| B. | 0.1 mol/L Na2SO4溶液中,含有SO42- 数为0.1NA | |
| C. | 92 g NO2和N2O4混合气体中含有氧原子总数为4NA | |
| D. | 标况下,22.4升SO3含有原子总数为4 NA |
1.根据键能数据(H-Cl 431kJ/mol,H-I 297kJ/mol),可得出的结论是( )
| A. | HI比HCl稳定 | |
| B. | HI比HCl熔、沸点高 | |
| C. | 溶于水时,HI比HCl更容易电离,所以氢碘酸是强酸 | |
| D. | 拆开等物质的量的HI和HCl,HI消耗的能量多 |
8.常温下,下列溶液pH=2的是( )
| A. | 0.01 mol•L-1 CH3COOH溶液 | |
| B. | 10-3 mol•L-1 H2SO4浓缩到原体积的10倍. | |
| C. | pH=1的H2SO4溶液稀释10倍 | |
| D. | c(OH-)=10-2 mol•L-1 的某溶液 |
5.设NA为阿伏加德罗常数的值,下列判断正确的是( )
| A. | 含4molHCl的浓盐酸与足量MnO2混合加热,产生NA个Cl2 | |
| B. | 标准状况下,22.4L己烷中共价键数为19NA | |
| C. | 0.1mol Fe与0.1mol Cl2充分反应,转移的电子数为0.3 NA | |
| D. | 氧气和臭氧组成的4.8g混合气体中含有0.3 NA个氧原子 |
6.分类是化学学习和研究的常用手段,下列分类依据和结论都正确的是( )
| A. | HCHO、Al2O3均含有氧元素,属于氧化物 | |
| B. | H2SO4、HNO3均为强酸,属于强电解质 | |
| C. | 蓝宝石、明矾的主要成分都是含有铝元素的氧化物 | |
| D. | AlCl3、Na2O2都属于离子化合物 |
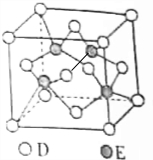 原子序数递增的主族元素A、B、C、D、E,已知B的单质是生活中最常见的金属之一,该元素与同主族元素A、D原子的核电荷数分别相差8和18,C元素的最高价氧化物的水化物属于最强无机酸,E与D同周期,E的气态基态原子第一电离能大于同周期相邻主族元素.
原子序数递增的主族元素A、B、C、D、E,已知B的单质是生活中最常见的金属之一,该元素与同主族元素A、D原子的核电荷数分别相差8和18,C元素的最高价氧化物的水化物属于最强无机酸,E与D同周期,E的气态基态原子第一电离能大于同周期相邻主族元素.