题目内容
下列说法正确的是( )
A. 只含H、N、O三种元素的化合物,可能是离子化含物,也可能是共价化合物。
B. 元素周期表中,ⅠA族与ⅦA族元素间只能形成离子化合物。
C. NaHCO3、CH3COONa均含有离子键和共价键。
D. 化合物MgO、SiO2、SO3中化学键的类型相同。
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案工业上用矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)获取铜和胆矾的操作流程如下:
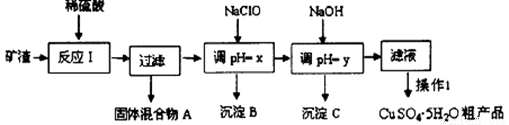
已知:①部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
②B、C均为单一沉淀
请回答下列问题:
(1)已知Cu2O在酸性条件下发生自身氧化还原反应,写出离子反应方程式______________。
(2)为了加快反应I的速率,可以采取的措施是______________(写1点)。
(3)固体混合物A中的成分是__________________________。
(4)反应I完成后,铁元素的存在形式为_______________(填离子符号);写出生成该离子的离子方程式___________________________________。
(5)x对应的数值范围是_______________________。用NaClO调pH,生成沉淀B的反应的离子方程式为____________________________________。
(6)已知:Ksp[Al(OH)3]=1.1×10-33,当调节溶液的pH为5时,c(Al3+)=_________ mol•L-1
(7)洗涤CuSO4·5H2O粗产品不能用大量水洗,而用冰水洗涤.原因是___________________。
在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)  M(g)+N(g),所得实验数据如下表:
M(g)+N(g),所得实验数据如下表:
实验编号 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量 /mol | |
n(X) | n(Y) | n(M) | ||
① | 700 | 0.40 | 0.10 | 0.090 |
② | 800 | 0.10 | 0.40 | 0.080 |
③ | 800 | 0.20 | 0.30 | a |
④ | 900 | 0.10 | 0.15 | b |
下列说法正确的是
A. 实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,用N表示的平均反应速率υ(N)=1.0×10-2mol/(L·min)
B. 实验②中,该反应的平衡常数K=2.0
C. 实验③中,达到平衡是,X的转化率为60%
D. 实验④中,达到平衡时,b>0.060

 2NH3的可逆反应中,自反应开始至2s末,氨的浓度由0变为0.4mol•L-1,则以氢气的浓度变化表示该反应在2 s内的平均反应速率是
2NH3的可逆反应中,自反应开始至2s末,氨的浓度由0变为0.4mol•L-1,则以氢气的浓度变化表示该反应在2 s内的平均反应速率是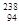 Pu作为热源材料。下列关于
Pu作为热源材料。下列关于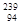 Pu具有相同的最外层电子数
Pu具有相同的最外层电子数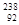 U具有完全相同的化学性质
U具有完全相同的化学性质