题目内容
气体A、B分别为0.6mol和0.5mol,在0.4L密闭容器中发生反应:3A+B?aC+2D,经5min后,此时C为0.2mol,又知在此反应时间内,D的平均反应速率为0.1mol?(L?min)-1,下列结论正确的是( )
| A、此时,反应混合物总的物质的量为1mol |
| B、B的转化率为50% |
| C、A的平均反应速率为0.1mol?(L?min)-1 |
| D、a值为2 |
考点:化学平衡的计算
专题:化学平衡专题
分析:根据三段式计算出各组分物质的量变化量、平衡时物质的量,
A.根据平衡时各自的物质的量求出总的物质的量;
B.根据三段式计算可得;
C.根据v=
=
计算v(A);
D.利用化学计量数之比等于变化的物质的量之比计算x.
A.根据平衡时各自的物质的量求出总的物质的量;
B.根据三段式计算可得;
C.根据v=
| △c |
| △t |
| △n |
| V?△t |
D.利用化学计量数之比等于变化的物质的量之比计算x.
解答:
解:经5min后,此时气体C为0.2mol,D的平均反应速率为0.1mol/(L?min),生成D的物质的量为0.1mol/(L?min)×5min×0.4L=0.2mol,则:
3A+B?aC+2D,
起始量(mol) 0.6 0.5 0 0
变化量(mol) 0.3 0.1 0.2 0.2
5min后(mol) 0.3 0.4 0.2 0.2
A.此时,反应混合物总物质的量为1.1mol,故A错误;
B.B的转化率为
×100%=20%,故B错误;
C.v(A)═
=
=
=0.15mol/(L?min),故C错误;
D.物质的量之比等于化学计量数之比,故0.2:0.2=a:2,则x=2,故D正确;
故选D.
3A+B?aC+2D,
起始量(mol) 0.6 0.5 0 0
变化量(mol) 0.3 0.1 0.2 0.2
5min后(mol) 0.3 0.4 0.2 0.2
A.此时,反应混合物总物质的量为1.1mol,故A错误;
B.B的转化率为
| 0.1mol |
| 0.5mol |
C.v(A)═
| △c |
| △t |
| △n |
| V?△t |
| 0.3mol |
| 0.4L×5min |
D.物质的量之比等于化学计量数之比,故0.2:0.2=a:2,则x=2,故D正确;
故选D.
点评:本题考查了化学平衡的计算,注意对速率公式的理解与灵活运用,注意三段式理清数据关系,难度中等.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列关于pH=3的盐酸和醋酸溶液的说法正确的是( )
| A、两种溶液中由水电离出来的c(H+)不相同 |
| B、中和相同体积的两种酸溶液所需NaOH的物质的量相同 |
| C、加入等质量的铁粉,反应过程中放出H2的速率相同 |
| D、分别用蒸馏水稀释m倍和n倍,两溶液pH仍相同,则m<n |
下列物质:①H3O+ ②[B(OH)4]- ③CH3COO ④NH3 ⑤CH4⑥NH4+中存在配位键的是( )
| A、①②⑥ | B、①③⑤ |
| C、③④⑤ | D、②④⑥ |
温度为T℃,压强为1.01×106Pa条件下,某密闭容器内,下列反应达到化学平衡A(g)+B(g)?3C,测得此时c(A)=0.022mol/L:压缩容器使压强增大到2.02×106Pa,第二次达到平衡时,测得 c(A)=0.05mol/L;若继续压缩容器,使压强增大到4.04×106Pa,第三次达到平衡时,测得 c(A)=0.075mol/L.则下列关于C物质状态的推测正确的是( )
| A、C为非气态 |
| B、C为气态 |
| C、第二次达到平衡时C为气态 |
| D、第三次达到平衡时 C为气态 |
依托孕烯是一种激素类药物,结构如图所示.下列有关依托孕烯的说法正确的是( )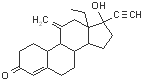

| A、依托孕烯的分子式为C21H28O2 |
| B、依托孕烯能与FeCl3溶液发生显色反应 |
| C、l mol依托孕烯最多能与5mol氢气发生加成反应 |
| D、依托孕烯能发生氧化、加成、消去、酯化等反应 |
下列溶液中,与100ml 0.5mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是( )
| A、100 ml 0.5 mol/L MgCl2 溶液 |
| B、200 ml 0.25 mol/L HCl溶液 |
| C、200 ml 0.25 mol/L CaCl2溶液 |
| D、50 ml 1 mol/L NaCl溶液 |
