题目内容
1.下列说法不正确的是( )| A. | 物质发生化学反应都伴随着能量变化 | |
| B. | 化学反应中能量变化的大小与反应物的质量密切相关 | |
| C. | 中和反应的反应热可以通过实验测得 | |
| D. | 实验法是获取反应热数据的唯一方法 |
分析 A、化学变化一定伴随着能量的变化;
B、化学反应中的能量变化与物质的质量成正比;
C、可以通过中和反应热的实验来测定中和热的数值;
D、很多反应的反应热不能通过实验测定.
解答 解:A、化学变化一定伴随着能量的变化,但有能量变化的不一定是化学反应,故A正确;
B、化学反应中的能量变化与参与反应的物质的物质的量、质量均成正比,即参与反应的物质的量或质量越多,则反应的能量变化越大,故B正确;
C、可以通过中和反应热的实验来测定中和热的数值,即中和热的数值可以通过实验测得,故C正确;
D、很多反应的反应热不能通过实验测定,但可以通过盖斯定律来计算得到,故实验法不是获取反应热数据的惟一的方法,故D错误.
故选D.
点评 本题考查了化学反应中的能量变化,注意由于很多反应的反应热不能通过实验直接测定,可以通过盖斯定律来计算得到.

练习册系列答案
相关题目
8.“分子机器设计和合成”有着巨大的研究潜力.人类步入分子器件时代后,使得光控、温控和电控分子的能力更强,如图是蒽醌套索醚电控开关.下列说法错误的是( )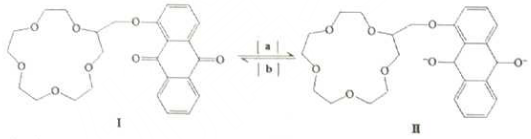

| A. | 物质Ⅰ的分子式是C25H28O8 | B. | 反应[a]是氧化反应 | ||
| C. | 1molⅠ可与8molH2发生加成反应 | D. | 物质Ⅰ的所有原子不可能共平面 |
9.下列有关物质的性质与用途具有对应关系的是( )
| A. | 铝具有良好导热性,可用铝罐贮运浓硝酸 | |
| B. | 水玻璃能与酸反应,可用作生产黏合剂和防火剂 | |
| C. | NaNO2具有碱性,可用于使铁零件表面生成Fe3O4 | |
| D. | FeCl3溶液能与Cu反应,可用作铜制线路板的蚀刻剂 |
16.下列事实,不能用勒夏特列原理解释的是( )
| A. | 向氯水中加入AgNO3溶液后,溶液颜色变浅 | |
| B. | 对2HI(g)?H2(g)+I2(g)平衡体系,体积缩小,压强增大可使颜色变深 | |
| C. | 合成氨反应中用过量氮气与氢气反应可以提高氢气的转化率 | |
| D. | 将混合气中的氨气液化后不停的分离出来,有利于合成氨的反应 |
6.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,11.2 L H2O含有的分子数为0.5NA | |
| B. | 常温常压下,11.2 L CO2 含有的分子数为0.5NA | |
| C. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2 L | |
| D. | 25℃、1.01×105Pa下,64 g SO2 中含有的原子数为3NA |
10.下列对“改变反应条件,导致化学反应速率改变”的原因描述不正确的是( )
| A. | 升高温度能使化学反应速率增大,主要原因是增加了活化分子的百分数,从而使有效碰撞频率提高 | |
| B. | 增大气体反应的压强,单位体积中活化分子数增多,气体反应速率加快 | |
| C. | 增大反应物的浓度,活化分子百分数增加,反应速率加快 | |
| D. | 催化剂通过改变反应路径,使反应所需的活化能降低,反应速率增大 |

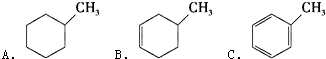
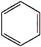 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$ +HBr.
+HBr.