题目内容
14.下列各组有机物只用一种试剂无法鉴别的是( )| A. | 乙醇、甲苯、硝基苯 | B. | 苯、四氯化碳、己烯 | ||
| C. | 苯、甲苯、环己烷 | D. | 乙酸乙酯、溴苯、乙酸 |
分析 A.利用水及分层现象可鉴别;
B.利用溴水可以鉴别;
C.苯、环己烷性质稳定,密度都比水小;
D.利用水及分层现象可鉴别.
解答 解:A.乙醇溶于水,甲苯、硝基苯都不溶于水,甲苯密度比水小,硝基苯密度比水大,可用水鉴别,故A不选;
B.甲苯、四氯化碳都不溶于水,甲苯密度比水小,四氯化碳密度比水大,己烯可与溴水反应,可用溴水鉴别,故B不选;
C.苯、环己烷性质稳定,密度都比水小,用一种试剂无法鉴别,故C选;
D.乙酸溶于水,乙酸乙酯、溴苯都不溶于水,乙酸乙酯密度比水小,溴苯密度比水大,可用水鉴别,故D不选.
故选C.
点评 本题考查有机物的鉴别,为高频考点,把握常见有机物的性质及反应中的现象为解答的关键,注意现象相同不能鉴别物质,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.应:N2(g)+3H2?2NH3(g).已知反应过程中某一时刻N2、H2、NH3浓度为0.1mol/L、0.3mol/L、0.2mol/L.当反应达到平衡时可能存在的数据是( )
| A. | N2为0.2mol/L,H2为0.6mol/L | B. | N2为0.15mol/L | ||
| C. | N2、H2均为0.18mol/L | D. | NH3为0.4mol/L |
5.自然环境与人们的生活息息相关.下列有关环境问题的说法不正确的是( )
| A. | 氟利昂(CCl2F2)因破坏大气臭氧层而导致“温室效应” | |
| B. | 将垃圾分类并回收利用是垃圾处理的发展方向 | |
| C. | 废旧电池的回收,其主要目的是保护环境,而不是回收金属 | |
| D. | 淀粉餐具被认为是有发展前景的一次性餐具,可有利于保护环境 |
2.下列说法正确的是( )
| A. | 1mol任何气体的体积都是22.4L | |
| B. | 1mol H2的质量是1g,它所占的体积是22.4L | |
| C. | 在标准状况下,1mol任何气体所占的体积都约为22.4L•mol-1 | |
| D. | 在标准状况下,1mol任何气体所占的体积都约为22.4L |
9.根据你所学习的元素周期律和周期表知识回答下列相关问题:
(1)现有部分短周期元素的性质或原子结构如表:
①元素Y的氢化物的电子式为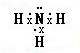 ,其水溶液呈碱性的原因是(用电离方程式表示):NH3•H2O?NH4++OH-.
,其水溶液呈碱性的原因是(用电离方程式表示):NH3•H2O?NH4++OH-.
②元素Z与元素T相比,非金属性较强的是Cl(填元素符号).
③探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是H2CO3(填化学式).
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质).把与下面元素有关的性质相符的曲线标号填入相应的空格中:

①ⅡA族元素的最外层电子数(填字母)b.
②第三周期元素的最高化合价(填字母)c.
③N3-、O2-、F-、Na+、Mg2+、Al3+的离子半径(填字母)a.
(3)周期表中某些元素化合物的易燃性、毒性变化有一定规律性,例如:
①氢化物的易燃性:第二周期CH4>NH3>H2O>HF;
第三周期SiH4>PH3>H2S>HCl(填化学式).
②化合物的毒性:PH3>NH3,H2S>H2O.CS2>CO2,(选填>、<或=).
(1)现有部分短周期元素的性质或原子结构如表:
| 元素编号 | 元素性质或原子结构 |
| T | 单质是一种淡黄色固体,是黑火药成分之一 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
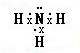 ,其水溶液呈碱性的原因是(用电离方程式表示):NH3•H2O?NH4++OH-.
,其水溶液呈碱性的原因是(用电离方程式表示):NH3•H2O?NH4++OH-.②元素Z与元素T相比,非金属性较强的是Cl(填元素符号).
③探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是H2CO3(填化学式).
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质).把与下面元素有关的性质相符的曲线标号填入相应的空格中:

①ⅡA族元素的最外层电子数(填字母)b.
②第三周期元素的最高化合价(填字母)c.
③N3-、O2-、F-、Na+、Mg2+、Al3+的离子半径(填字母)a.
(3)周期表中某些元素化合物的易燃性、毒性变化有一定规律性,例如:
①氢化物的易燃性:第二周期CH4>NH3>H2O>HF;
第三周期SiH4>PH3>H2S>HCl(填化学式).
②化合物的毒性:PH3>NH3,H2S>H2O.CS2>CO2,(选填>、<或=).
19.取一定质量的均匀固体混合物Cu、Cu2O和CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g,另一份加入1000mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为( )
| A. | 3.2mol/L | B. | 1.6mol/L | C. | 0.9mol/L | D. | 无法判断 |
6.化学与生活、社会密切相关,下列说法正确的是( )
| A. | SO2可以用来漂白纸浆、毛、丝、草帽辫、增白食品等 | |
| B. | 通信光缆的主要成分是晶体Si,太阳能电池的材料主要是SiO2 | |
| C. | 高锰酸钾溶液、酒精、双氧水都能杀菌消毒,都利用了强氧化性 | |
| D. | 氨很容易液化,液氨气化吸收大量的热,所以液氨常用作致冷剂 |
4.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1mol•L-1的NaCl 溶液中含有Cl-的数目为NA | |
| B. | 78g 苯含有C=C双键的数目为3NA | |
| C. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| D. | 标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
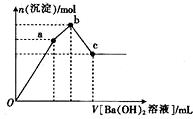 甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成.甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子.A元素原子核内质子数比E的少l,D、E同主族.某同学为探究甲的组成而进行如下实验:
甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成.甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子.A元素原子核内质子数比E的少l,D、E同主族.某同学为探究甲的组成而进行如下实验: