��Ŀ����
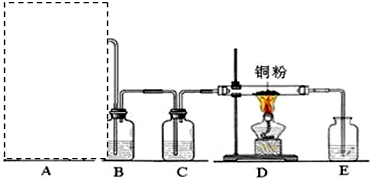
20��A��һ����Ҫ�Ļ���ԭ�ϣ�������ܶ�1.25g/L��C��һ���������ʣ�D�Ǿ��й�����ζ�����������A��B��C��D��һ�������´�������ת����ϵ��ʯ���ͺ�17��̼ԭ�����ϵ�Һ̬���������ַ�Ӧ���������ﱻʡ�ԣ���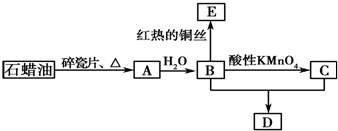
д�����б仯�Ļ�ѧ����ʽ��ָ����Ӧ���ͣ�
��A��B��CH2�TCH2+H2O $��_{���ȼ�ѹ}^{����}$CH3CH2OH���ӳɷ�Ӧ��
��B+C��D��CH3COOH+CH3CH2OH $��_{��}^{ŨH_{2}SO_{4}}$CH3COOCH2CH3+H2O��������ȡ������Ӧ��
���� A��һ����Ҫ�Ļ���ԭ�ϣ��ڱ�״���µ��ܶ�Ϊ1.25g/L����Mr��A��=1.25��22.4=28����AΪCH2=CH2��CH2=CH2��ˮ��һ�������·����ӳɷ�Ӧ����BΪCH3CH2OH��CH3CH2OH���������Ը����������������CΪCH3COOH��CH3CH2OH��CH3COOH��Ũ���������·�Ӧ����DΪCH3COOCH2CH3��CH3CH2OH��������������EΪCH3CHO���Դ˽����⣮
��� �⣺A��һ����Ҫ�Ļ���ԭ�ϣ��ڱ�״���µ��ܶ�Ϊ1.25g/L����Mr��A��=1.25��22.4=28����AΪCH2=CH2��CH2=CH2��ˮ��һ�������·����ӳɷ�Ӧ����BΪCH3CH2OH��CH3CH2OH���������Ը����������������CΪCH3COOH��CH3CH2OH��CH3COOH��Ũ���������·�Ӧ����DΪCH3COOCH2CH3��CH3CH2OH��������������EΪCH3CHO��
��A��B��CH2=CH2��ˮ��һ�������·����ӳɷ�Ӧ����CH3CH2OH����Ӧ����ʽΪ��CH2�TCH2+H2O $��_{���ȼ�ѹ}^{����}$CH3CH2OH��
��B+C��D���������Ҵ�����������Ӧ����������������Ӧ����ʽΪ��CH3COOH+CH3CH2OH $��_{��}^{ŨH_{2}SO_{4}}$CH3COOCH2CH3+H2O��Ҳ����ȡ����Ӧ��
�ʴ�Ϊ��CH2�TCH2+H2O $��_{���ȼ�ѹ}^{����}$CH3CH2OH���ӳɷ�Ӧ��CH3COOH+CH3CH2OH $��_{��}^{ŨH_{2}SO_{4}}$CH3COOCH2CH3+H2O��������ȡ������Ӧ��
���� ���⿼���л����ƶϡ��л���Ӧ���͡�ͬ���칹��ȣ��漰ϩ�봼������֮���ת����ϵ�ȣ��ѶȲ���ע�����֪ʶ���������գ�

 �����������Ů��ͯ������ϵ�д�
�����������Ů��ͯ������ϵ�д�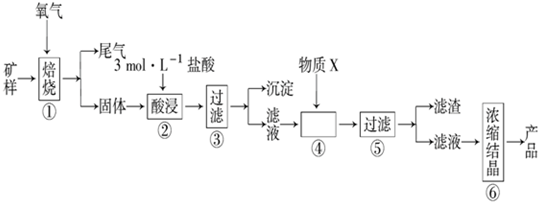
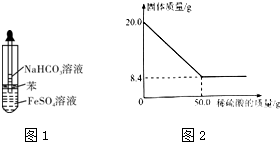
��֪�������£��������ӿ�ʼ�����ͳ�����ȫʱ��pH �����
| ���� ���� | �������↑ʼ������pH | �������������ȫ��pH |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
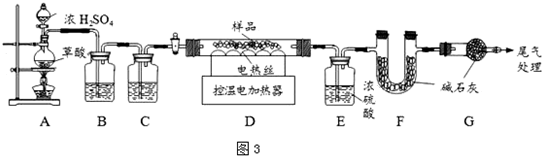
��l������ٵı��չ�������Ҫͨ����������ʵ�����У���ʹ�ó�����ѧ����������ͼ��ʾװ����ȡ��������д����Ϥ�ķ�������������������ѧ����ʽ��2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2 ����2Na2O2+2H2O=4NaOH+O2����
��2�����ղ�����β���к��е�һ���������γ��������Ⱦ�����β��ͨ�백ˮ�У��ܷ��������Ӧ��д�����п��ܷ���������������ԭ��Ӧ�Ļ�ѧ����ʽ��2��NH4��2SO3+O2�T2��NH4��2SO4��2NH4HSO3+O2�T2NH4HSO4��
��3���������������У���Ҫ�õ�3mol•L-1������100mL�����Ƹ�������Һʱ�������õ��ձ�������������ͷ�ι��⣬����Ҫ��������100ml������ƿ����Ͳ��
��4������ܼ�������X��Ŀ���ǿ�����Һ��pH��ʹFe3+�Գ�������ʽȫ������������X ����ѡ�����������е�D��
��A���������ơ���B��ϡ���ᡡ��C����ˮ����D������ͭ
��5������Һ�н�������Ũ�ȵ���1��10-5 mol•L-1ʱ����Ϊ�ý������ӳ�����ȫ����Ksp[Fe��OH��2]=1��10-15��
| A�� | �ӳ����ʯ��ˮ | B�� | ���߷ֱ���ͬŨ�ȵ�ϡ���ᷴӦ | ||
| C�� | ����ˮ���Ƚ����ܽ��� | D�� | ���߷ֱ����NaOH��Һ |
| A�� | 2H2��g��+O2��g��=2H2O��l������H=-142.9 kJ•mol-1 | |
| B�� | H2��g��+$\frac{1}{2}$O2��g��=H2O��l������H=-285.8 kJ•mol-1 | |
| C�� | 2H2+O2=2H2O����H=-571.6 kJ•mol-1 | |
| D�� | H2��g��+$\frac{1}{2}$O2��g��=H2O��g������H=-285.8 kJ•mol-1 |
| A�� | ���ݷ�ɢϵ�Ƿ���ж��������ɢϵ��Ϊ��Һ���������Һ | |
| B�� | ����������к��е���ԭ�Ӹ����ɽ����ΪһԪ�ᡢ��Ԫ�ᡢ��Ԫ��� | |
| C�� | þ���Ͻ�Ư�ۡ�ˮ��������ˮ��Ϊ����� | |
| D�� | �����ʯ�ҡ����ᡢʳ��ˮ��Ϊ����� |