题目内容
 氮是一种非常重要的元素,它的单质和化合物应用广泛,在科学技术和生产中有重要的应用.砷(As)位于周期表中的第4周期,与氮元素属同一主族元素,其广泛分布于自然界.试回答下列问题:
氮是一种非常重要的元素,它的单质和化合物应用广泛,在科学技术和生产中有重要的应用.砷(As)位于周期表中的第4周期,与氮元素属同一主族元素,其广泛分布于自然界.试回答下列问题:(1)砷的气态氢化物的电子式为
(2)NA表示阿伏加德罗常数的数值.46gNO2和N2O4的混合气体中含有
(3)氨和联氨(N2H4)是氮的两种常见化合物,制备联氨可用丙酮为催化剂,将次氯酸钠与氨气反应,该反应中还原剂与氧化剂的物质的量之比为2:1,写出该反应的化学方程式
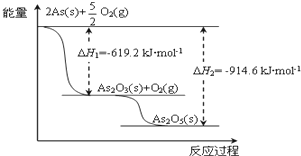
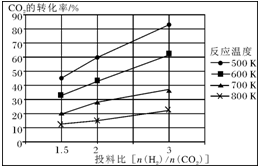
(4)砷的常见酸性氧化物有As2O3和As2O5,请根据图相关信息写出As2O5分解为As2O3的热化学方程式
(5)直接供氨式碱性燃料电池的电池反应式是4NH3+3O2=2N2+6H2O,电解质溶液一般使用KOH溶液,则负极电极反应式是
考点:物质的量的相关计算,氧化还原反应,热化学方程式,化学电源新型电池
专题:计算题,基本概念与基本理论
分析:(1)砷的气态氢化物为AsH3,结构类似于氨气,非金属性As<N,元素的非金属性越强,对应的氢化物越稳定;
(2)根据n=
=
结合分子构成计算;
(3)次氯酸钠与氨气反应,根据NaClO氧化NH3可以得到肼来书写方程式;
(4)由图象可知As2O3生成As2O5的反应热为(-914.6kJ/mol+619.2kJ/mol)=-295.4kJ/mol,以此可计算As2O5分解为As2O3的反应热;
(5)碱性条件下,氨气被氧化生成N2和水.
(2)根据n=
| m |
| M |
| N |
| NA |
(3)次氯酸钠与氨气反应,根据NaClO氧化NH3可以得到肼来书写方程式;
(4)由图象可知As2O3生成As2O5的反应热为(-914.6kJ/mol+619.2kJ/mol)=-295.4kJ/mol,以此可计算As2O5分解为As2O3的反应热;
(5)碱性条件下,氨气被氧化生成N2和水.
解答:
解:(1)砷的气态氢化物为AsH3,结构类似于氨气,电子式为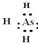 ,非金属性As<N,元素的非金属性越强,对应的氢化物越稳定,则稳定性比NH3弱,
,非金属性As<N,元素的非金属性越强,对应的氢化物越稳定,则稳定性比NH3弱,
故答案为: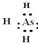 ;弱;
;弱;
(2)NO2和N2O4的最简式都为NO2,则46gNO2和N2O4的混合气体中含有
=1molN原子,则N原子个数为1NA,
NO2和CO2的分子组成相似,则分子总数为NA个的NO2和CO2混合气体含2NA个氧原子数,
15N中质子数为7,中子数为15-7=8,则1mol15N中,中子数比质子数多1NA个,
1L 1mol/LFe(NO3)3溶液中含3NA个NO3-离子,
故答案为:1;2;1;3;
(3)制备肼的方法,是以NaClO氧化NH3,反应中还原剂与氧化剂的物质的量之比为2:1,制得肼的稀溶液,反应为NaClO+2NH3═N2H4+H2O+NaCl,故答案为:NaClO+2NH3=N2H4+NaCl+H2O;
(4)由图象可知As2O3生成As2O5的反应热为(-914.6kJ/mol+619.2kJ/mol)=-295.4kJ/mol,则As2O5分解为As2O3的反应热为+295.4kJ/mol,
所以热化学方程式为As2O5(s)=As2O3(s)+O2(g)△H=+295.4 kJ?mol-1,
故答案为:As2O5(s)=As2O3(s)+O2(g)△H=+295.4 kJ?mol-1;
(5)碱性条件下,氨气被氧化生成N2和水,方程式为2NH3+6OH--6e-=N2+6H2O,故答案为:2NH3+6OH--6e-=N2+6H2O.
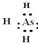 ,非金属性As<N,元素的非金属性越强,对应的氢化物越稳定,则稳定性比NH3弱,
,非金属性As<N,元素的非金属性越强,对应的氢化物越稳定,则稳定性比NH3弱,故答案为:
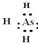 ;弱;
;弱;(2)NO2和N2O4的最简式都为NO2,则46gNO2和N2O4的混合气体中含有
| 46g |
| 46g/mol |
NO2和CO2的分子组成相似,则分子总数为NA个的NO2和CO2混合气体含2NA个氧原子数,
15N中质子数为7,中子数为15-7=8,则1mol15N中,中子数比质子数多1NA个,
1L 1mol/LFe(NO3)3溶液中含3NA个NO3-离子,
故答案为:1;2;1;3;
(3)制备肼的方法,是以NaClO氧化NH3,反应中还原剂与氧化剂的物质的量之比为2:1,制得肼的稀溶液,反应为NaClO+2NH3═N2H4+H2O+NaCl,故答案为:NaClO+2NH3=N2H4+NaCl+H2O;
(4)由图象可知As2O3生成As2O5的反应热为(-914.6kJ/mol+619.2kJ/mol)=-295.4kJ/mol,则As2O5分解为As2O3的反应热为+295.4kJ/mol,
所以热化学方程式为As2O5(s)=As2O3(s)+O2(g)△H=+295.4 kJ?mol-1,
故答案为:As2O5(s)=As2O3(s)+O2(g)△H=+295.4 kJ?mol-1;
(5)碱性条件下,氨气被氧化生成N2和水,方程式为2NH3+6OH--6e-=N2+6H2O,故答案为:2NH3+6OH--6e-=N2+6H2O.
点评:本题考查较为综合,涉及多方面的知识,贴近高考,注意把握物质的构成特点以及热化学方程式的书写,难度中等.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
短周期元素W、X、Y、Z的原子序数依次增大,W与Y,X与Z分别位于同一主族,W与X可形成两种常见气体WX2和WX,Y原子的内层电子总数是其最外层电子数的2.5倍,下列叙述中不正确的是( )
| A、WX2分子中所有原子最外层都已满足8电子结构 |
| B、WX2、ZX2的化学键类型相同 |
| C、原子半径大小顺序为:X<W<Y<Z |
| D、乙醇、乙酸、葡萄糖、油脂中均含W、X两种元素 |
下列实验操作或装置符合实验要求的是( )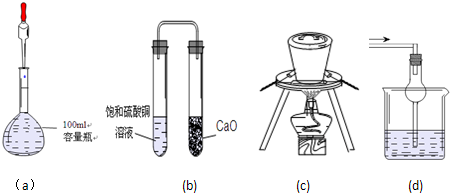

| A、(a) 可用于定容并量取15.00 mL NaOH溶液 |
| B、(b)装置放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
| C、(c)可用于高温煅烧石灰石 |
| D、(d)可用于易溶于水的尾气吸收 |
 燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等. 水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得:
水煤气(CO 和H2)是重要燃料和化工原料,可用水蒸气通过炽热的炭层制得: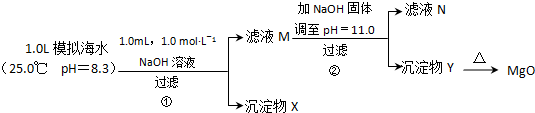
 如图中各物质均由常见元素(原子序数≤20)组成.已知A、B、K为单质,且在常温下A和K为气体,B为固体.D为常见的无色液体.I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生.J是一种实验室常用的干燥剂.它们的相互转化关系如图所示(图中反应条件未列出).
如图中各物质均由常见元素(原子序数≤20)组成.已知A、B、K为单质,且在常温下A和K为气体,B为固体.D为常见的无色液体.I是一种常用的化肥,在其水溶液中滴加AgNO3溶液有不溶于稀HNO3的白色沉淀产生.J是一种实验室常用的干燥剂.它们的相互转化关系如图所示(图中反应条件未列出).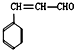 和化合物Ⅱ
和化合物Ⅱ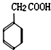 在一定条件下发生反应能生成化合物Ⅲ
在一定条件下发生反应能生成化合物Ⅲ ,请回答以下问题.
,请回答以下问题. )代替两个NH3与铂配位,则生成的产物
)代替两个NH3与铂配位,则生成的产物 和氯化钠溶液反应制取
和氯化钠溶液反应制取  的离子反应方程式
的离子反应方程式 )及呋喃(
)及呋喃( )形成的配合物[Pt(C4H4O)(C4H5N)Cl2],写出其结构简式
)形成的配合物[Pt(C4H4O)(C4H5N)Cl2],写出其结构简式