题目内容
5.下列说法正确的是( )| A. | FeSO4溶液存放在加有少量铁粉的试剂瓶中 | |
| B. | 将1mol/L的NaCl溶液保存在容量瓶中 | |
| C. | 凡是给玻璃仪器加热,都要垫石棉网,以防仪器炸裂 | |
| D. | 用pH试纸检验某溶液的酸碱性时,一定要先用蒸馏水湿润 |
分析 A.亚铁离子具有较强还原性,存放硫酸亚铁溶液时需要加入铁粉防止被氧化;
B.不能在容量瓶中保存溶液;
C.有的玻璃仪器可以直接加热,如试管;
D.pH试纸沉淀溶液酸碱性时不能润湿,否则可能影响测定结果.
解答 解:A.FeSO4中Fe为+2价,易被氧化为+3价,加入铁粉后,会与+3价的铁反应使之成为亚铁离子,反应FeSO4溶液存放在加有少量铁粉的试剂瓶中,故A正确;
B.容量瓶只能用于配制一定浓度的溶液,不能存放溶液,故B错误;
C.给试管加热时不需要垫上石棉网,可以直接加热,故C错误;
D.用pH试纸检验某溶液的酸碱性时,若先用蒸馏水湿润,待测液被稀释,测定的酸溶液的pH偏大、碱溶液的pH减小,故D错误;
故选A.
点评 本题考查了化学实验方案的评价,题目难度不大,涉及溶液配制、pH试纸的使用、溶液保存等知识,明确常见仪器构造及使用方法为解答关键,试题培养了学生的分析能力及化学实验能力.

练习册系列答案
相关题目
16.为了检验某固体物质中是否含有NH4+,一定用不到的试剂或试纸是( )
| A. | NaOH溶液 | B. | 浓盐酸 | C. | 稀硫酸 | D. | 红色石蕊试纸 |
13.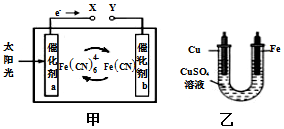 甲是一种太阳能电池的工作原理示意图,电解质为K3[Fe(CN)6]和K4[Fe(CN)6]的混合溶液,将甲装置和乙装置相连实现铁件上镀铜.下列说法正确的是( )
甲是一种太阳能电池的工作原理示意图,电解质为K3[Fe(CN)6]和K4[Fe(CN)6]的混合溶液,将甲装置和乙装置相连实现铁件上镀铜.下列说法正确的是( )
 甲是一种太阳能电池的工作原理示意图,电解质为K3[Fe(CN)6]和K4[Fe(CN)6]的混合溶液,将甲装置和乙装置相连实现铁件上镀铜.下列说法正确的是( )
甲是一种太阳能电池的工作原理示意图,电解质为K3[Fe(CN)6]和K4[Fe(CN)6]的混合溶液,将甲装置和乙装置相连实现铁件上镀铜.下列说法正确的是( )| A. | 电池工作时,K+移向电极a | |
| B. | 电极b表面发生的电极反应Fe(CN)64--e-═Fe(CN)63- | |
| C. | Cu电极应与Y相连接,发生氧化反应 | |
| D. | 工作一段时间后,甲乙两装置中电解质溶液浓度均变小 |
20.下列过程对应的离子方程式正确的是( )
| A. | NaHSO3溶于水呈酸性:NaHSO3═Na++H++SO32- | |
| B. | 在Na2S2O3溶液中滴加稀硫酸:2H++S2O32-═SO2↑+S↓+H2O | |
| C. | 浓盐酸与MnO2反应制氯气:MnO2+4HCl═Mn2++2Cl2+2H2O | |
| D. | 工业冶炼Mg:2Mg2++2O2-$\frac{\underline{\;电解\;}}{\;}$2Mg+O2↑ |
10.下列气体的制备和性质实验中,由现象得出的结论正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向二氧化锰固体中加入浓盐酸后加热,将产生的气体通入淀粉碘化钾溶液液 | 溶液变蓝 | Cl2具有氧化性 |
| B | 向亚硫酸钠固体中加入浓硫酸,将产生的气体通入溴水 | 溴水褪色 | SO2具漂白性 |
| C | 向蔗糖溶液中加稀硫酸,水浴加热后,加入新制氢氧化铜,加热 | 溶液变蓝 | 蔗糖水解产物没有还原性 |
| D | 无水乙醇与浓硫酸共热170℃,将产生的气体通入酸性高锰酸钾溶液 | 溶液褪色 | 乙烯可被化酸性高锰酸钾氧化 |
| A. | A | B. | B | C. | C | D. | D |
17.下列事实不能用化学平衡移动原理解释的是( )
| A. | 收集氯气用排饱和食盐水的方法 | |
| B. | 加压条件下有利于SO2和O2反应生成SO3 | |
| C. | 将NO2球浸泡在热水中颜色加深 | |
| D. | 加催化剂,使N2和H2在一定的条件下转化为NH3 |
14.下列说法正确的是( )
| A. | 蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 | |
| B. | 生活中常见金属镁、铝、铁、铜等均能通过热还原法冶炼 | |
| C. | 胶体具有介稳性,是因为同种胶体粒子的运动有规律,即布朗运动 | |
| D. | 由于2NO+2CO?2CO2+N2的△H<0,则该反应一定能自发进行 |