题目内容
 某小组查阅资料得知:C2O42-+MnO4-+H+→CO2↑+Mn2++H2O(未配平),欲利用该反应测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数.该小组称量1.34g草酸钠样品溶于稀硫酸中,然后用0.200mol?L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应).
某小组查阅资料得知:C2O42-+MnO4-+H+→CO2↑+Mn2++H2O(未配平),欲利用该反应测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数.该小组称量1.34g草酸钠样品溶于稀硫酸中,然后用0.200mol?L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应).(1)滴定前是否要滴加指示剂?
(2)滴定时用
(3)达到终点时消耗了15.00mL的高锰酸钾溶液,样品中草酸钠的质量分数为
考点:中和滴定
专题:实验题
分析:(1)根据酸性高锰酸钾溶液为紫红色,过程中不需要加指示剂;
(2)根据酸性高锰酸钾溶液具有强氧化性;
(3)在酸性条件下,高锰酸根离子能和草酸发生氧化还原反应生成二价锰离子、二氧化碳和水,根据反应计算.
(2)根据酸性高锰酸钾溶液具有强氧化性;
(3)在酸性条件下,高锰酸根离子能和草酸发生氧化还原反应生成二价锰离子、二氧化碳和水,根据反应计算.
解答:
解:(1)酸性高锰酸钾溶液为紫红色,当达到滴定终点时,再滴入酸性高锰酸钾溶液时,紫红色不再褪去,
故答案为:否;酸性高锰酸钾溶液为紫红色,达滴定终点紫色不再褪去;
(2)酸性高锰酸钾溶液具有强氧化性,腐蚀橡皮管,应用酸式滴定管,
故答案为:b;
(3)草酸钠(Na2C2O4)溶于稀硫酸中,然后用酸性高锰酸钾溶液进行滴定,消耗n(KMnO4)=0.015L×0.200mol?L-1=3×10-3mol,离子方程式为:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O,则
2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O.
2 5
3×10-3mol 7.5×10-3mol
样品中草酸钠的质量为m=7.5×10-3mol×134g/mol=7.5×134×10-3g,
样品中草酸钠的质量分数为
×100%=75%,
故答案为:75%.
故答案为:否;酸性高锰酸钾溶液为紫红色,达滴定终点紫色不再褪去;
(2)酸性高锰酸钾溶液具有强氧化性,腐蚀橡皮管,应用酸式滴定管,
故答案为:b;
(3)草酸钠(Na2C2O4)溶于稀硫酸中,然后用酸性高锰酸钾溶液进行滴定,消耗n(KMnO4)=0.015L×0.200mol?L-1=3×10-3mol,离子方程式为:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O,则
2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O.
2 5
3×10-3mol 7.5×10-3mol
样品中草酸钠的质量为m=7.5×10-3mol×134g/mol=7.5×134×10-3g,
样品中草酸钠的质量分数为
| 7.5×134×10-3g |
| 1.34g |
故答案为:75%.
点评:该题涉及到氧化还原滴定,虽然基于反应原理与中和滴定不同,但实验原理及操作和所用仪器等类似,由于该反应有明显的颜色变化,故可不用指示剂.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
下列各组离子中,在给定条件下能大量共存的是( )
| A、c(NO3-)=1mol?L-1的溶液中:NH4+、Ba2+、Fe2+、Br- |
| B、水电离出c(OH-)=10-10mol?L-1的溶液:HCO3-、K+、Na+、Cl- |
| C、在pH=2的溶液中:NH4+、K+、ClO-、Cl- |
| D、c(Fe3+)=0.1mol?L-1的溶液中:K+、ClO-、SO42-、SCN- |
下列实验方案中,能测定Na2CO3和NaHCO3混合物中NaHCO3质量分数的是( )
①取a克混合物充分加热,减重b克
②取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
③取a克混合物与足量稀酸充分反应,逸出气体先用浓硫酸干燥再用碱石灰吸收,碱石灰增重b克
④取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体.
①取a克混合物充分加热,减重b克
②取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体
③取a克混合物与足量稀酸充分反应,逸出气体先用浓硫酸干燥再用碱石灰吸收,碱石灰增重b克
④取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体.
| A、只有①②④ | B、①②③④ |
| C、只有①③④ | D、只有①②③ |
下列表示溶液中所发生反应的离子方程式正确的是( )
A、NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH-
| ||||
| B、Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+H2O | ||||
| C、KI溶液与H2SO4酸化的H2O2溶液混合:2I-+H2O2+2H+═2H2O+I2 | ||||
| D、向氯化银悬浊液中加入饱和碘化钾溶液:Ag++I-═AgI↓ |
已知反应I2(g)+H2(g)?2HI(g)△H<0,下列说法正确的是( )
| A、降低温度,正向反应速率减小倍数大于逆向反应速率减小倍数 |
| B、升高温度将缩短达到平衡的时间 |
| C、达到平衡后,保持温度和容积不变,充入氩气,正、逆反应速率同等倍数增大 |
| D、达到平衡后,保持温度和压强不变,充入氩气,HI的质量将减小 |
下列对sp3、sp2、sp杂化轨道的夹角的比较,得出结论正确的是( )
| A、sp杂化轨道的夹角最大 |
| B、sp2杂化轨道的夹角最大 |
| C、sp3杂化轨道的夹角最大 |
| D、sp3、sp2、sp杂化轨道的夹角相等 |
含有C=C的有机物与O3作用形成不稳定的臭氧化物,臭氧化物在还原剂存在下,与水作用分解为羰基化合物,总反应为:

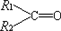 +
+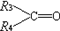 (R1、R2、R3、R4为H或烷基)
(R1、R2、R3、R4为H或烷基)
以下四种物质发生上述反应,所得产物为纯净物且能发生银镜反应的是( )

| (O3)Zn/H2O |
 +
+ (R1、R2、R3、R4为H或烷基)
(R1、R2、R3、R4为H或烷基)以下四种物质发生上述反应,所得产物为纯净物且能发生银镜反应的是( )
| A、(CH3)2C=C(CH3)2 |
B、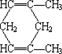 |
C、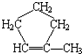 |
D、 (环锌四烯) (环锌四烯) |




 分别代表有关反应中的一种物质,请填写以下空白.
分别代表有关反应中的一种物质,请填写以下空白.