题目内容
有一澄清透明溶液,只可能含有大量H+、Fe3+、Fe2+、Al3+、AlO2-、CO32-、NO3-七种离子中的几种,向溶液中逐滴加入一定量1mol/L的NaOH溶液的过程中,开始没有沉淀,而后有沉淀,沉淀达最大量后继续滴加NaOH溶液沉淀部分消失.下列判断正确的是
A.一定不含Fe3+和Fe2+
B.一定含有Al3+,Fe3+、Fe2+至少含有一种或两种皆有
C.溶液可能含有NO3-
D.一定含有Fe3+ ,但一定不含Fe2+
D
【解析】
试题分析:根据题意知,向该溶液中加入一定量1mol/L NaOH溶液的过程中,开始没有沉淀,说明溶液中一定含有大量的H+离子,在酸性溶液中AlO2-、CO32-离子分别与H+离子反应生成Al(OH)3沉淀、CO2气体而不能存在;根据溶液的电中性可知,溶液中一定含有NO3-离子;在酸性条件下Fe2+离子与NO3-离子发生氧化还原反应而不能共存,则溶液中一定不含Fe2+离子;而后有沉淀,沉淀达最大量后继续滴加NaOH溶液沉淀部分消失,说明溶液中一定含有Al3+和Fe3+;综上所述,溶液中一定含有H+、NO3- 、Fe3+、Al3+,一定没有AlO2-、CO32-、Fe2+离子;A、根据上述分析知,溶液中一定含Fe3+,一定不含有Fe2+,错误;B、根据上述分析知,Fe2+一定不存在,错误;C、根据上述分析知,溶液中一定存在NO3-,错误;D、根据上述分析知,溶液中一定含Fe3+,一定不含有Fe2+,正确。
考点:考查离子检验和离子推断。

练习册系列答案
相关题目
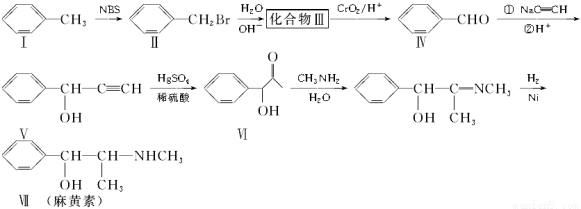
 xC(g),△H<0。测得两容器中c(A)随时间t的变化如图所示:
xC(g),△H<0。测得两容器中c(A)随时间t的变化如图所示: