题目内容
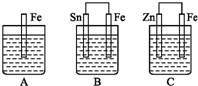 A,、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如图所示:
A,、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸,如图所示:(1)A中反应的离子方程式为
(2)B中Sn极的电极反应式为
(3)C中被氧化的金属是
考点:原电池和电解池的工作原理
专题:
分析:(1)铁与稀硫酸反应生成硫酸亚铁和氢气;
(2)Fe比Sn活泼,Fe为负极,Sn为正极,负极发生氧化反应,正极发生还原反应;
(3)Zn比Fe活泼,锌被腐蚀,为原电池负极,铁为正极,电化学腐蚀的速率大于化学腐蚀的速率,金属做原电池正极时得到保护.
(2)Fe比Sn活泼,Fe为负极,Sn为正极,负极发生氧化反应,正极发生还原反应;
(3)Zn比Fe活泼,锌被腐蚀,为原电池负极,铁为正极,电化学腐蚀的速率大于化学腐蚀的速率,金属做原电池正极时得到保护.
解答:
解:(1)铁与硫酸反应的离子方程式为:Fe+2H+=Fe2++H2↑,故答案为:Fe+2H+=Fe2++H2↑;
(2)铁比锡活泼,锡为原电池正极,电极反应式为:2H++2e-=H2↑;氢离子浓度减小,溶液的pH值增大,故答案为:2H++2e-=H2↑;升高;
(3)锌比铁活泼,锌为原电池负极,被氧化,负极电极反应式为Zn-2e-=Zn2+,正极:2H++2e-=H2↑,总反应方程式为Zn+2H+=Zn2++H2↑,
故答案为:Zn;Zn+2H+=Zn2++H2↑.
(2)铁比锡活泼,锡为原电池正极,电极反应式为:2H++2e-=H2↑;氢离子浓度减小,溶液的pH值增大,故答案为:2H++2e-=H2↑;升高;
(3)锌比铁活泼,锌为原电池负极,被氧化,负极电极反应式为Zn-2e-=Zn2+,正极:2H++2e-=H2↑,总反应方程式为Zn+2H+=Zn2++H2↑,
故答案为:Zn;Zn+2H+=Zn2++H2↑.
点评:本题考查金属的电化学腐蚀与防护,题目难度不大,注意金属的电化学腐蚀与化学腐蚀的区别,以及比较金属腐蚀快慢的方法.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、实验室用大理石和稀盐酸制取二氧化碳:2H++CO32-=CO2↑+H2O |
| B、氯气与碘化钾溶液的反应:Cl2+2 I-=2Cl-+I2 |
| C、向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-=Al(OH)3↓ |
| D、三氯化铁溶液中加入铜粉:Fe3++Cu═Fe+Cu 2+ |
铊(81T1)是元素周期表ⅢA族元素,下列关于铊的叙述不正确的是( )
| A、铊比铝的金属性更强 |
| B、铊能与盐酸反应放出氢气 |
| C、铊在化合物中可以是+3价 |
| D、氢氧化铊一定具有两性 |
下列说法正确的是( )
| A、吸热反应都需加热才能发生 |
| B、在铁制品上镀铜时,铁制品作阳极,铜盐溶液作电镀液 |
| C、应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D、密闭容器中进行的可逆反应,气体压强不发生变化时说明反应一定达到化学平衡状态 |
向13.6gCu和Cu2O的混合物中加入某浓度的稀硝酸0.25L,固体物质完全反应,生成NO和Cu(NO3)2.在所得溶液中加入0.5mol/L的NaOH溶液1L,反应后溶液恰好呈中性,金属离子已完全沉淀,沉淀质量为19.6g,下列说法不正确的是( )
| A、Cu与Cu2O的物质的量之比为2:1 |
| B、硝酸的物质的量浓度为2 mol/L |
| C、Cu、Cu2O与硝酸反应后剩余HNO3的物质的量为0.5mol |
| D、产生的NO在标准状况下的体积为2.24L |