题目内容
元素周期表中第三周期元素的单质及其化合物的用途广泛.
(1)该周期元素中,半径最小的简单离子的离子结构示意图为 .
(2)能证明氯的非金属性(得电子能力)比硫强的化学方程式为 .
(3)NaHSO3溶液呈酸性,其溶液中离子浓度由大到小的顺序为 .
(4)ClO2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ClO2被还原为Cl-,该反应的离子方程式为 .
(5)已知下列两反应过程中能量变化如图所示:
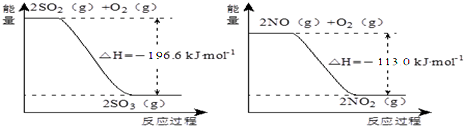
汽车尾气中含有的少量NO2和SO2在一定条件下会发生反应,该反应的热化学方程式为 .
(1)该周期元素中,半径最小的简单离子的离子结构示意图为
(2)能证明氯的非金属性(得电子能力)比硫强的化学方程式为
(3)NaHSO3溶液呈酸性,其溶液中离子浓度由大到小的顺序为
(4)ClO2可将弱酸性废水中的Mn2+转化为MnO2而除去,同时ClO2被还原为Cl-,该反应的离子方程式为
(5)已知下列两反应过程中能量变化如图所示:

汽车尾气中含有的少量NO2和SO2在一定条件下会发生反应,该反应的热化学方程式为
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:(1)从Na+到Al3+,P3-到Cl-半径也分别依次减小,半径最小的金属离子是铝离子;
(2)氯气单质能把S从其化合物中置换出来,证明氯气氧化性强于S;
(3)NaHSO3溶液呈酸性,NaHSO3溶液中存在亚硫酸氢根的水解与电离,水解导致其呈碱性,电离导致其呈酸性,据此分析:电离程度大于水解程度;
(4)ClO2氧化除去Mn2+生成MnO2,ClO2反应后的产物为Cl-,以此书写离子方程式即可;
(5)依据盖斯定律计算即可.
(2)氯气单质能把S从其化合物中置换出来,证明氯气氧化性强于S;
(3)NaHSO3溶液呈酸性,NaHSO3溶液中存在亚硫酸氢根的水解与电离,水解导致其呈碱性,电离导致其呈酸性,据此分析:电离程度大于水解程度;
(4)ClO2氧化除去Mn2+生成MnO2,ClO2反应后的产物为Cl-,以此书写离子方程式即可;
(5)依据盖斯定律计算即可.
解答:
解:(1)从Na+到Al3+,P3-到Cl-半径也分别依次减小,半径最小的金属离子是铝离子,其离子结构示意图为 ,故答案为:
,故答案为: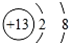 ;
;
(2)氯气单质能把S从其化合物中置换出来,证明氯气氧化性强于S,化学反应方程式为:Cl2+H2S=S↓+2HCl 故答案为:Cl2+H2S=S↓+2HCl;
(3)NaHSO3溶液呈酸性,NaHSO3溶液中存在亚硫酸氢根的水解与电离,水解导致其呈碱性,电离导致其呈酸性,据此分析:电离程度大于水解程度;故离子浓度大小为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-),故答案为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-);
(4)ClO2氧化除去Mn2+生成MnO2,ClO2反应后的产物为Cl-,该反应的离子方程式为:2 ClO2+5Mn2++6H2O=5MnO2 ↓+2Cl-+12H+,故答案为:2 ClO2+5Mn2++6H2O=5MnO2 ↓+2Cl-+12H+;
(5)依据O2(g)+2SO2(g)=2SO3(g)△H=-196.6kJ?mol-1 ①;2NO(g)+O2(g)=2NO2(g)△H=-113.0kJ?mol-1 ②故
(①-②)得:NO2(g)+SO2(g)=NO(g)+SO3(g)△H=-41.8kJ?mol-1 ,故答案为:NO2(g)+SO2(g)=NO(g)+SO3(g)△H=-41.8kJ?mol-1.
 ,故答案为:
,故答案为: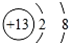 ;
;(2)氯气单质能把S从其化合物中置换出来,证明氯气氧化性强于S,化学反应方程式为:Cl2+H2S=S↓+2HCl 故答案为:Cl2+H2S=S↓+2HCl;
(3)NaHSO3溶液呈酸性,NaHSO3溶液中存在亚硫酸氢根的水解与电离,水解导致其呈碱性,电离导致其呈酸性,据此分析:电离程度大于水解程度;故离子浓度大小为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-),故答案为:c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-);
(4)ClO2氧化除去Mn2+生成MnO2,ClO2反应后的产物为Cl-,该反应的离子方程式为:2 ClO2+5Mn2++6H2O=5MnO2 ↓+2Cl-+12H+,故答案为:2 ClO2+5Mn2++6H2O=5MnO2 ↓+2Cl-+12H+;
(5)依据O2(g)+2SO2(g)=2SO3(g)△H=-196.6kJ?mol-1 ①;2NO(g)+O2(g)=2NO2(g)△H=-113.0kJ?mol-1 ②故
| 1 |
| 2 |
点评:本题综合考查了离子半径大小比较、离子浓度大小比较、氧化还原反应方程式书写、盖斯定律等,有一定难度.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、乙醇分子可以看作是乙烷分子中的一个氢原子被-OH取代而形成的 |
| B、乙醇分子中的氢原子都可以被钠置换 |
| C、-OH和OH-两种微粒中质子数、电子数都相等 |
| D、水和乙醇分子中的羟基化学性质完全相同 |
洁净煤技术(Clean Coal Technology,简称CCT)的含义是:旨在减少污染和提高效率的煤炭加工、燃烧、转化和污染控制等新技术的总称.下列措施不属于洁净煤技术的是( )
| A、选煤厂溶剂萃取脱硫 |
| B、煤的气化(产物主要为CO和H2) |
| C、将煤在氢气和催化剂作用下通过加氢裂化转变为液体燃料的过程 |
| D、发电厂用燃煤发电 |
下列变化只涉及物理变化的是( )
| A、煤的干馏 | B、石油的裂化 |
| C、石油的分馏 | D、乙烯聚合 |
25℃时,三种难溶银盐的Ksp与颜色如表,下列说法正确的是( )
| AgCl | Ag2CrO4 | AgI | |
| 颜色 | 白 | 砖红 | 黄 |
| Ksp | 1.8×10-10 | 1.0×10-12 | 8.5×10-17 |
| A、AgCl、Ag2CrO4、AgI饱和溶液中c(Ag+)依次减弱 |
| B、Ag2CrO4饱和溶液中c(Ag+)约为1.0×10-6mol?L-1 |
| C、向AgCl悬浊液加入足量KI溶液,沉淀将由白色转化为黄色 |
| D、向等浓度的KCl与K2CrO4混合溶液中滴加少量AgNO3溶液,将生成砖红色沉淀 |
下列说法中错误的是( )
| A、熔融状态下能够导电的化合物中一定存在离子键 |
| B、单原子形成的离子,一定与稀有气体原子的核外电子排布相同 |
| C、L层上的电子数为奇数的原子一定是主族元素的原子 |
| D、同一主族的元素的原子,最外层电子数相同,化学性质不一定完全相同 |
 .
.