题目内容
在锌跟稀硝酸反应时,若参加反应的锌与消耗的硝酸的物质的量之比为1:2.5时,则被还原的HNO3和未被还原HNO3的物质的量之比为( )
| A、2:5 | B、1:4 |
| C、1:5 | D、1:9 |
考点:氧化还原反应的计算
专题:氧化还原反应专题
分析:生成硝酸锌时HNO3未被还原,参加反应的锌与消耗的硝酸的物质的量之比为1:2.5时,设物质的量分别为1mol、2.5mol,结合原子守恒和电子守恒来计算.
解答:
解:生成硝酸锌时HNO3未被还原,参加反应的锌与消耗的硝酸的物质的量之比为1:2.5时,设物质的量分别为1mol、2.5mol,则生成硝酸锌时未被还原HNO3的物质的量为2mol,
设硝酸的还原产物中N元素的化合价为n,若被还原的硝酸的物质的量为2.5mol-2mol=0.5mol,
由电子守恒可知,1mol×(2-0)=0.5mol×(5-n),解得n=+1,
即生成N2O时,则被还原的HNO3和未被还原HNO3的物质的量之比为0.5mol:2mol=1:4,
若生成硝酸铵时,发生4Zn+10HNO3=4Zn(NO3)2+NH4NO3+3H2O,被还原的HNO3和未被还原HNO3的物质的量之比为1:(8+1)=1:9,
故选BD.
设硝酸的还原产物中N元素的化合价为n,若被还原的硝酸的物质的量为2.5mol-2mol=0.5mol,
由电子守恒可知,1mol×(2-0)=0.5mol×(5-n),解得n=+1,
即生成N2O时,则被还原的HNO3和未被还原HNO3的物质的量之比为0.5mol:2mol=1:4,
若生成硝酸铵时,发生4Zn+10HNO3=4Zn(NO3)2+NH4NO3+3H2O,被还原的HNO3和未被还原HNO3的物质的量之比为1:(8+1)=1:9,
故选BD.
点评:本题考查氧化还原反应的计算,为高频考点,把握反应中电子守恒和原子守恒的应用为解答的关键,侧重分析与计算能力的考查,选项D易漏选,题目难度中等.

练习册系列答案
相关题目
下列实验操作中,所用仪器合理为是( )
| A、用体温表测量沸水的温度 |
| B、用100 mL的量筒量取5.2mL的盐酸 |
| C、用托盘天平称取25.2 g NaCl |
| D、用100mI容量瓶配制50mL0.1mol/L的盐酸 |
在水溶液中能大量共存的一组离子是( )
| A、Fe2+、Al3+、ClO-、Cl- |
| B、NH4+、Na+、I-、CO32- |
| C、K+、HCO3-、OH-、NO3- |
| D、Fe2+、H+、SO42-、NO3- |
已知室温时,0.1mol/L某一元酸HA在水中有0.1%发生电离,下列叙述不正确的是( )
①该溶液的pH=4;
②升高温度,溶液的pH增大;
③此酸的电离平衡常数约为1×10-7;
④加水稀释后,各离子的浓度均减小;
⑤由HA电离出的c(H+)约为水电离出的c(H+)的106倍;
⑥适当增大HA的浓度,HA的电离平衡正向移动,电离平衡常数增大.
①该溶液的pH=4;
②升高温度,溶液的pH增大;
③此酸的电离平衡常数约为1×10-7;
④加水稀释后,各离子的浓度均减小;
⑤由HA电离出的c(H+)约为水电离出的c(H+)的106倍;
⑥适当增大HA的浓度,HA的电离平衡正向移动,电离平衡常数增大.
| A、②④⑥ | B、①④⑤ |
| C、②⑤⑥ | D、②④⑤ |
以下化学用语正确的是( )
| A、苯的最简式 C6H6 |
| B、乙醇的分子式CH3CH2OH |
| C、乙烯的结构简式CH2CH2 |
| D、乙炔的结构简式:CH≡CH |
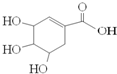 “达菲”瑞士罗氏制药公司生产的一种治疗禽流感和甲型H1N1流感(猪流感)的特效药.达菲的主要有效成分莽草酸是从中国百姓常见的调味料八角茴香中提取出来的.莽草酸的结构式如图,下列说法正确的是( )
“达菲”瑞士罗氏制药公司生产的一种治疗禽流感和甲型H1N1流感(猪流感)的特效药.达菲的主要有效成分莽草酸是从中国百姓常见的调味料八角茴香中提取出来的.莽草酸的结构式如图,下列说法正确的是( )| A、它的分子式为C7H7O5 |
| B、遇FeCl3溶液呈紫色 |
| C、它不能发生消去反应 |
| D、1mol莽草酸跟足量的钠反应可以得到2molH2 |
下列除去杂质的方法不正确的是( )
| A、镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 |
| B、用过量氨水除去Fe3+溶液中的少量Al3+ |
| C、Al(OH)3中混有少量Mg(OH)2:加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO2后过滤 |
| D、MgO中混有少量Al2O3:加入足量烧碱溶液,充分反应,过滤、洗涤、干燥得到MgO |
下列物质互为同分异构体的一组是( )
| A、35Cl和 37 Cl |
| B、正丁烷和异丁烷 |
| C、O2和 O3 |
| D、H2O 和 H2O2. |
用铁片与稀硫酸反应制氢气时,下列措施不能使氢气生成速率加大的是( )
| A、加热 |
| B、不用稀硫酸,改用98%浓硫酸 |
| C、加水稀释硫酸 |
| D、不用铁片,改用铁粉 |