题目内容
Na2O 23.9g溶于 g水中所得溶液中
=
.
| n(Na+) |
| n(H2O) |
| 1 |
| 10 |
考点:物质的量的相关计算
专题:计算题
分析:先求出 23.9gNa2O中含有的钠离子的物质的量,根据氧化钠与水反应消耗的水的物质的量以及根据溶液中
=
得到溶液中水的物质的量,然后根据m=nM计算质量.
| n(Na+) |
| n(H2O) |
| 1 |
| 10 |
解答:
解:23.9gNa2O中n(Na+)=2n(Na2O)=2×
=0.77mol,氧化钠与水反应消耗的水为0.385mol,根据溶液中
=
得到溶液中水的物质的量为7.7mol,因此共需要水8.085mol,其质量为8.085mol×18g/mol=145.5g,
故答案为:145.5.
| 23.9g |
| 62g/mol |
| n(Na+) |
| n(H2O) |
| 1 |
| 10 |
故答案为:145.5.
点评:本题考查了物质的量的相关计算,题目难度一般,注意不能忽略了氧化钠与水反应消耗的水的物质的量.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质的主要成分正确的是( )
| A、赤铁矿:Fe3O4 |
| B、小苏打:NaHCO3 |
| C、磁铁矿:Fe2O3 |
| D、明矾:KAl(SO4)2 |
已知自然界氧的同位素160、17O、18O,碳酸钙的同位素有16C、18C,从二氧化碳酸饮料分子的原子组成来看.自然界的CO2一共有( )
| A、3种 | B、6种 | C、9种 | D、12种 |
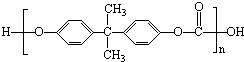 2010年5月1日上海世博会隆重开幕,世博会的环保概念是人们关心的话题,环保材料更为世人瞩目,其中聚碳酸酯是用得较多的材料.聚碳酸酯的结构简式如图所示,下列说法正确的是( )
2010年5月1日上海世博会隆重开幕,世博会的环保概念是人们关心的话题,环保材料更为世人瞩目,其中聚碳酸酯是用得较多的材料.聚碳酸酯的结构简式如图所示,下列说法正确的是( )| A、它在结构上可以看成由碳酸和另一有机物通过缩聚反应而成 |
| B、该有机物是一种高分子化合物,肯定易溶于水 |
| C、它是一种纯净物,属于酯类物质 |
| D、它耐强酸,强碱,不可与强氧化剂发生反应 |