题目内容
4.乙醇转化为乙醛,发生的反应为( )| A. | 取代反应 | B. | 加成反应 | C. | 消除反应 | D. | 氧化反应 |
分析 乙醇在催化条件下,可与氧气反应生成乙醛,以此解答该题.
解答 解:乙醇在催化条件下,可与氧气反应生成乙醛,-OH被氧化生成-CHO,为氧化反应,
故选D.
点评 本题考查有机物的结构和性质,为高频考点,侧重考查学生的分析能力,注意把握官能团的变化和反应类型的判断,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.化学实验安全处理不正确的是( )
| A. | 苯酚沾在皮肤上用大量水冲洗 | |
| B. | 金属钠着火时,立即用沙子盖灭 | |
| C. | 制备氯气时,应用NaOH溶液吸收多余的氯气 | |
| D. | 制备乙烯时向乙醇和浓硫酸的混合液中加碎瓷片 |
15.下列变化过程需要吸收能量的是( )
| A. | 甲烷的燃烧 | B. | H2→H+H | C. | 酸碱中和反应 | D. | CaO+H2O=Ca(OH)2 |
12.在某元素的原子核外电子排布中,K电子层和L电子层的电子数之和等于M电子层和N电子层的电子数之和.则该元素的核电荷数为( )
| A. | 12 | B. | 17 | C. | 20 | D. | 30 |
19.燃料电池是一种新型电池.某氢氧燃料电池的基本反应是:X极:O2(g)+2H2O(l)+4e-=4OH-Y极:2H2(g)-4e-+4OH-=4H2O(l)下列判断正确的是( )
| A. | 该电池的电解质溶液为酸性 | B. | 电池总反应为2H2+O2=2H2O | ||
| C. | X极是负极,发生氧化反应 | D. | 电池工作一段时间后溶液PH增大 |
9.在给定的条件下,下列选项所示的物质间转化均能实现的是( )
| A. | Al2O3$\stackrel{盐酸}{→}$AlCl3溶液$\stackrel{通电}{→}$Al | |
| B. | NH3$→_{△}^{O_{2}/催化剂}$NO2$\stackrel{H_{2}O}{→}$HNO3 | |
| C. | S$→_{点燃}^{O_{2}}$SO2$\stackrel{H_{2}O}{→}$H2SO4 | |
| D. | SiO2$\stackrel{NaOH溶液}{→}$Na2SiO3溶液$\stackrel{CO_{2}}{→}$H2SiO3 |
16.通过以下反应均可获取H2.下列有关说法不正确的是( )
①太阳光催化分解水制氢:2H2O(1)═2H2(g)+O2(g)△H1=+571.6kJ/mol
②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=+131.3kJ/mol
③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.1kJ/mol( )
①太阳光催化分解水制氢:2H2O(1)═2H2(g)+O2(g)△H1=+571.6kJ/mol
②焦炭与水反应制氢:C(s)+H2O(g)═CO(g)+H2(g)△H2=+131.3kJ/mol
③甲烷与水反应制氢:CH4(g)+H2O(g)═CO(g)+3H2(g)△H3=+206.1kJ/mol( )
| A. | 由反应①知H2的燃烧热为571.6kJ/mol | |
| B. | 反应②中生成物的总能量高于反应物的总能量 | |
| C. | 反应③若改用新催化剂,△H3不变化 | |
| D. | 反应CH4(g)═C(s)+2H2(g)的△H=+74.8kJ/mol |
8.表是元素周期表的一部分,下列有关说法不正确的是( )
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | a | b | |||||
| 3 | c | d | e | f |
| A. | 元素 a 是制备一种高效电池的重要材料 | |
| B. | 由于分子间氢键的作用,同族中由 b 元素形成的氢化物沸点是最高的 | |
| C. | c、d 两元素的单质构成原电池两电极时,d 可能为负极 | |
| D. | e、f 的含氧酸的酸性依次增强 |
9.下列实验方案设计正确的是( )
| A. | 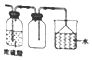 利用图收集干燥的氯化氢气体 | |
| B. | 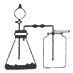 选择合适的试剂,利用图2可分别制取并收集少量CO2、NO和O2 | |
| C. |  利用图可验证铁发生吸氧腐蚀 | |
| D. |  利用图蒸干NH4Cl饱和溶液制备NH4Cl晶体 |