题目内容
14.下列离子方程式,正确的是( )| A. | 铜与盐酸反应:Cu+2H+═Cu2++H2↑ | |
| B. | 氧化铁与稀盐酸反应:Fe2O3+6H+═2Fe3++3H2O | |
| C. | 锌与硝酸银溶液反应:Zn+Ag+═Zn2++Ag | |
| D. | 在硫酸溶液中加入氢氧化钡溶液:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
分析 A、铜和盐酸不反应;
B、氧化铁和盐酸反应生成氯化铁和水;
C、离子方程式不符合电荷守恒;
D、离子方程式不符合离子配比.
解答 解:A、铜和盐酸不反应,故此离子方程式不符合实际,故A错误;
B、氧化铁和盐酸反应生成氯化铁和水,其中能拆的为盐酸和氯化铁,故离子方程式为Fe2O3+6H+═2Fe3++3H2O,故B正确;
C、离子方程式不符合电荷守恒,正确的是Zn+2Ag+═Zn2++2Ag,故C错误;
D、离子方程式不符合离子配比,当生成1mol硫酸钡时,生成2mol水,故正确的离子方程式为Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故D错误.
故选B.
点评 本题考查了离子方程式的书写,难度不大,应注意离子方程式应满足电荷守恒和离子配比.

练习册系列答案
相关题目
4.工业制硝酸中的一步重要反应是N2和H2在500℃时,高压、催化剂条件下反应:N2+3H2?2NH3,这是个正反应是放热的可逆反应.已知反应在密闭容器中进行,下列说法正确的是( )
| A. | 使用催化剂能加快反应速率,使N2完全转化为NH3 | |
| B. | 当N2、H2、NH3浓度相等时,反应达到化学平衡状态 | |
| C. | 一段时间后,当N2、H2、NH3浓度不再改变时,反应物转化率最大 | |
| D. | 达平衡后,升高温度,反应速率减慢 |
9.用NA表示阿伏加德罗常数的数值,则下列说法中不正确的是( )
| A. | 标准状况下,a L的氧气和氮气的混合物含有的分子数约为$\frac{a}{22.4}$×6.02×1023 | |
| B. | 由1L 1 mol•L-1的 FeCl3溶液制成的胶体中胶粒总数小于NA个 | |
| C. | 2.3g金属钠变为钠离子失去0.1NA电子 | |
| D. | 2.24L CO2中含有的原子数为3×0.1×6.02×1023 |
6.某同学通过一系列实验探究Cu及其化合物的性质,操作正确且能达到目的是( )
| A. | 将铜粉与硫粉混合均匀加热以制取CuS | |
| B. | 将铜丝插入浓硫酸中并加热,反应后再加水以观察CuSO4溶液的颜色 | |
| C. | 向CuSO4溶液中加入过量的NaOH溶液,过滤洗涤并收集沉淀充分灼烧以制取CuO | |
| D. | 向淀粉溶液中加入适量稀硫酸微热,再加少量新制Cu(OH)2并加热,产生砖红色沉淀 |
15.已知25℃时,AgCl的溶度积Ksp=1.8×10-10,则下列说法正确的是( )
| A. | 向饱和AgCl水溶液中加入盐酸,Ksp值变大 | |
| B. | AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) | |
| C. | 温度一定时,当溶液中c(Ag+)×c(Cl-)=Ksp时,此溶液中必有AgCl的沉淀析出 | |
| D. | 将AgCl加入到较浓的KI溶液中,AgCl能转化为AgI |
16.电解制金属锰的阳极泥中主要含有MnO2,MnO等.利用该阳极泥生产MnO2的工艺流程如下:
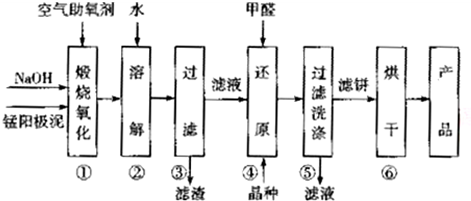
已知:①部分物质的溶解性或Ksp如表:
②Na2MnO4,在pH≤7的环境中,易歧化为MnO2和高锰酸钾.
回答下列问题:
(1)电解MnSO4溶液时,阴极为Mn2+得电子被还原为金属Mn,阳极反应式为2H2O-4e-=O2↑+4H+.
电解过程中溶液的pH不能过高,也不能过低,需要控制电解液的pH≈6.8,原因是pH过高,Mn2+生成Mn(OH)2,pH过低时,阴极上氢离子放电.
(2)步骤①中+2价Mn和+4价Mn均被氧化为Na2MnO4,写出该步骤中+2价Mn反应的化学方程式:MnO+2NaOH+O2$\frac{\underline{\;煅烧\;}}{\;}$Na2MnO4+H2O.
(3)步骤②一④均采用pH≈10的环境,目的是提高产品中Mn的转化率.
(4)步骤④中氧化剂与还原剂的物质的量之比为2:1,则氧化产物的化学式为CO2.该反应中除氧化产物和还原产物的另外一种生成物的化学式为NaOH.
(5)步骤⑥为烘干操作,所用的烘干设备可能是BD(填字母).
A.鼓风机 B.烘干机 C.压榨机 D.红外烘箱
(6)产率与步骤①煅烧温度的关系如图所示:
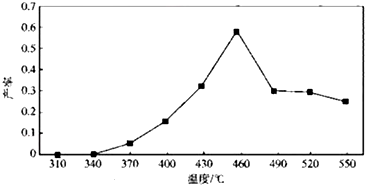
步骤①最好选用的煅烧温度约为B°C(填字母).
A.340 B.460 C.490 D.550.

已知:①部分物质的溶解性或Ksp如表:
| 物质 | MnSO4 | Mn(OH)2 | MnO2 |
| 溶解性或Ksp | 易溶 | 1.9×10-13 | 难溶 |
回答下列问题:
(1)电解MnSO4溶液时,阴极为Mn2+得电子被还原为金属Mn,阳极反应式为2H2O-4e-=O2↑+4H+.
电解过程中溶液的pH不能过高,也不能过低,需要控制电解液的pH≈6.8,原因是pH过高,Mn2+生成Mn(OH)2,pH过低时,阴极上氢离子放电.
(2)步骤①中+2价Mn和+4价Mn均被氧化为Na2MnO4,写出该步骤中+2价Mn反应的化学方程式:MnO+2NaOH+O2$\frac{\underline{\;煅烧\;}}{\;}$Na2MnO4+H2O.
(3)步骤②一④均采用pH≈10的环境,目的是提高产品中Mn的转化率.
(4)步骤④中氧化剂与还原剂的物质的量之比为2:1,则氧化产物的化学式为CO2.该反应中除氧化产物和还原产物的另外一种生成物的化学式为NaOH.
(5)步骤⑥为烘干操作,所用的烘干设备可能是BD(填字母).
A.鼓风机 B.烘干机 C.压榨机 D.红外烘箱
(6)产率与步骤①煅烧温度的关系如图所示:

步骤①最好选用的煅烧温度约为B°C(填字母).
A.340 B.460 C.490 D.550.
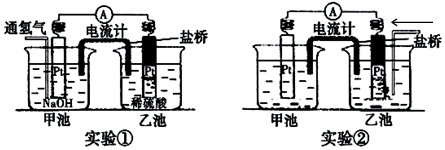
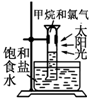
 .
.