题目内容
11.半水煤气是工业合成氨的原料气,其主要成分是H2、CO、CO2、N2和H2O(g).半水煤气经过下列步骤转化为合成氨的原料.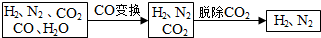
完成下列填空:
(1)半水煤气含有少量硫化氢.将半水煤气样品通入硝酸铅(或硫酸铜)溶液中(填写试剂名称),出现黑色沉淀,可以证明有硫化氢存在.
(2)半水煤气在铜催化下实现CO变换:CO+H2O$→_{△}^{Cu}$CO2+H2,若半水煤气中V(H2):V(CO):V(N2)=38:28:22,经CO变换后的气体中:V(H2):V(N2)=3:1.
(3)碱液吸收法是脱除二氧化碳的方法之一.已知:
| Na2CO3 | K2CO3 | |
| 20℃碱液最高浓度(mol/L) | 2.0 | 8.0 |
| 碱的价格(元/kg) | 1.25 | 9.80 |
(4)以下是测定半水煤气中H2以及CO的体积分数的实验方案.取一定体积(标准状况)的半水煤气,经过下列实验步骤测定其中H2以及CO的体积分数.
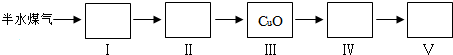
①选用合适的无机试剂分别填入Ⅰ、Ⅰ、Ⅳ、Ⅴ方框中.
②该实验方案中,步骤IV(选填“Ⅳ”或“Ⅴ”)可以确定半水煤气中H2的体积分数.
分析 (1)可以利用硫化氢与硝酸铅或硫酸铜等反应进行检验;
(2)反应中氮气体积不变,根据方程式计算生成氢气的体积,进而计算CO变换后的气体中氢气与氮气体积之比;
(3)碳酸钠比碳酸钾便宜,但碳酸钠溶液浓度比碳酸钾小,吸收二氧化碳的能力差;碳酸钾吸收二氧化碳生成碳酸氢钾,加热碳酸氢钾可以得到碳酸钾,再循环利用;
(4)①半水煤气中含有二氧化碳,首先利用碱液除去二氧化碳,干燥后再通过氧化铜反应,利用浓硫酸吸收产生的水蒸气,利用碱液吸收产生的二氧化碳,进而计算体积分数;
②氢气还原氧化铜生成水蒸气,浓硫酸吸收水蒸气.
解答 解:(1)将水煤气通入硝酸铅(或硫酸铜)溶液中,出现黑色沉淀,证明含有硫化氢,
故答案为:硝酸铅(或硫酸铜);黑色沉淀;
(2)若半水煤气中V(H2):V(CO):V(N2)=38:28:22,反应中氮气体积不变,根据方程式:CO+H2O$→_{△}^{Cu}$CO2+H2,可知经CO变换后的气体中V(H2):V(N2)=(38+28):22=3:1,
故答案为:3:1;
(3)碳酸钠比碳酸钾价格便宜,价廉,但碳酸钠溶液浓度比碳酸钾小,吸收二氧化碳的能力差;碳酸钾吸收二氧化碳生成碳酸氢钾,加热碳酸氢钾可以得到碳酸钾,再循环利用,反应方程式为:2KHCO3$\frac{\underline{\;\;△\;\;}}{\;}$K2CO3+CO2↑+H2O,
故答案为:价廉;吸收CO2能力差;碱液循环使用;2KHCO3$\frac{\underline{\;\;△\;\;}}{\;}$K2CO3+CO2↑+H2O;
(4)①半水煤气中含有二氧化碳,首先利用碱液除去二氧化碳,干燥后再通过氧化铜反应,利用浓硫酸吸收产生的水蒸气,利用碱液吸收产生的二氧化碳,进而计算体积分数,故流程图为: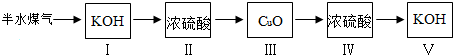 ,
,
故答案为: ;
;
②氢气还原氧化铜生成水蒸气,浓硫酸吸收水蒸气,故步骤IV可以确定半水煤气中H2的体积分数,
故答案为:IV.
点评 本题考查物质含量测定、气体检验、物质的分离提纯等,注意渗透实验中经济性,是对学生综合能力的考查.

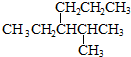 的命名正确的是( )
的命名正确的是( )| A. | 4-甲基-3-丙基戊烷 | B. | 3-异丙基己烷 | ||
| C. | 2-甲基-3-丙基戊烷 | D. | 2-甲基-3-乙基己烷 |
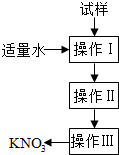
| A. | 操作Ⅰ是过滤,将固体分离除去 | |
| B. | 操作Ⅱ是加热浓缩.趁热过滤,除去杂质氯化钠 | |
| C. | 操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来 | |
| D. | 操作Ⅰ~Ⅲ总共需两次过滤 |
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
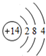 ,写出①的气态氢化物的分子式NH3.
,写出①的气态氢化物的分子式NH3.(2)元素③、⑩的最高价氧化物水化物的碱性最强的为KOH;元素②、⑧的氢化物稳定性最强的是HF;表中①-⑫化学性质最稳定的是Ar(均用化学式填空).
(3)在水溶液中⑧的单质与⑫的简单阴离子可发生反应,其离子方程式为:Cl2+2Br-=2Cl-+Br2.
(4)③、⑤两种元素的最高价氧化物的水化物的离子方程式是:Al(OH)3+OH-=AlO2-+2H2O.
| A. | 亚硫酸钠 | B. | 氢氧化钠 | C. | 过氧化钠 | D. | 碳酸氢钠 |
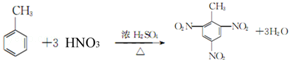
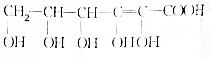 .
.
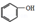 (制酚醛树脂)④
(制酚醛树脂)④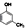 (生产杀虫剂)⑤CH2=CH─CH=CH2(合成橡胶原料)⑥HCHO(防腐剂)
(生产杀虫剂)⑤CH2=CH─CH=CH2(合成橡胶原料)⑥HCHO(防腐剂)