题目内容
实验室用乙醇和浓硫酸反应制备乙烯,化学方程式为:C2H5OH
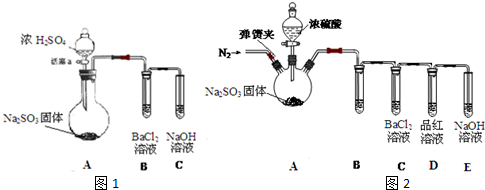
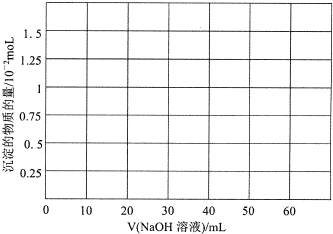
CH2=CH2↑+H2O;接着再用液溴与乙烯反应制备1,2-二溴乙烷.在制备过程中由于部分乙醇与浓硫酸发生氧化还原反应还会产生CO2、SO2,并进而与Br2反应生成HBr等酸性气体.某学习小组用上述三种为原料,组装下列仪器(短接口或橡皮管均己略去)来制备1,2-二溴乙烷

(1)如果气体流向从左到右,正确的连接顺序是:B经A①插入A中,D接入②;A③接 接 接 接 接.
(2)温度计水银球的正确位置是 .
(3)装置D与分流漏斗相比,其主要优点是 .
(4)装置C的主要作用是 ,装置F的作用是 .
(5)在反应管E中进行的主要反应的化学方程式为 .
(6)装置E烧杯中的泠水和反应管内液溴上的水层作用均是 .若将装置F拆除,在E中的主要反应为 .
| 浓硫酸 |
| 170℃ |

(1)如果气体流向从左到右,正确的连接顺序是:B经A①插入A中,D接入②;A③接
(2)温度计水银球的正确位置是
(3)装置D与分流漏斗相比,其主要优点是
(4)装置C的主要作用是
(5)在反应管E中进行的主要反应的化学方程式为
(6)装置E烧杯中的泠水和反应管内液溴上的水层作用均是
考点:乙醇的消去反应
专题:实验设计题
分析:解答过程需要注意两点:第一:必须除去混在乙烯中的气体杂质,尤其是SO2气体,以防止SO2与Br2发生反应SO2+Br2+2H2O=2HBr+H2SO4,影响1,2-二溴乙烷产品的制备;第二:必须在理解的基础上灵活组装题给的不太熟悉的实验仪器(如三颈烧瓶A、恒压滴液漏斗D、安全瓶防堵塞装置C),反应管E中冷水的作用是尽量减少溴的挥发,仪器组装顺序是:制取乙烯气体(用A、B、D组装)一安全瓶(C,兼防堵塞)→净化气体(F,用NaOH溶液吸收CO2和SO2等酸性杂质气体)→制备1,2-二溴乙烷的主要反应装置(E)→尾气处理(G)”,结合有机物的结构和性质以及题目要求可解答该题.
解答:
解:(1)仪器组装顺序为:制取乙烯气体(用A、B、D组装)→安全瓶(C,兼防堵塞)→净化气体(F,用NaOH溶液吸收CO2和SO2等酸性杂质气体)→制备1,2-二溴乙烷的主要反应装置(E)→尾气处理(G),
故答案为:C;F;E;G;
(2)乙醇在浓硫酸作用下加热到1700C时发消去反应生成乙烯,则温度计的位置应位于三颈瓶的液体中央,
故答案为:位于三颈瓶的液体中央;
(3)装置D为恒压滴液漏斗,该反应温度较高,容器内压强较大,若容器内压力过大时液体无法滴落,选用恒压滴液漏斗,可以平衡上下压强,使液体顺利滴下,
故答案为:平衡上下压强,使液体顺利滴下;
(4)装置C为安全瓶,起到防止倒吸的作用;乙醇与浓硫酸作用可生成CO2、SO2,为防止SO2与Br2发生反应SO2+Br2+2H2O=2HBr+H2SO4,影响1,2-二溴乙烷产品的制备,应用除去三颈瓶中产生的CO2、SO2,溴易挥发、有毒,为防止污染环境,应进行尾气处理,可用碱液吸收,
故答案为:防止倒吸;除去三颈瓶中产生的CO2、SO2,吸收挥发的溴蒸汽;
(5)在反应管E中进行的主要反应为乙烯和溴的加成反应,反应的方程式为:CH2=CH2+Br2→BrCH2CH2Br,
故答案为:CH2=CH2+Br2→BrCH2CH2Br;
(6)溴易挥发,为减少挥发,在反应管E中加入少量水可起到水封的作用,把反应管E置于盛有冷水的小烧杯中,可降低温度,减少挥发;
若将装置F拆除,乙烯中会混有二氧化硫,二氧化硫与溴单质反应生成硫酸和溴化氢,反应方程式为:SO2+Br2+H2O=H2SO4+2HBr,
故答案为:减少溴的挥发损失;SO2+Br2+H2O=H2SO4+2HBr.
故答案为:C;F;E;G;
(2)乙醇在浓硫酸作用下加热到1700C时发消去反应生成乙烯,则温度计的位置应位于三颈瓶的液体中央,
故答案为:位于三颈瓶的液体中央;
(3)装置D为恒压滴液漏斗,该反应温度较高,容器内压强较大,若容器内压力过大时液体无法滴落,选用恒压滴液漏斗,可以平衡上下压强,使液体顺利滴下,
故答案为:平衡上下压强,使液体顺利滴下;
(4)装置C为安全瓶,起到防止倒吸的作用;乙醇与浓硫酸作用可生成CO2、SO2,为防止SO2与Br2发生反应SO2+Br2+2H2O=2HBr+H2SO4,影响1,2-二溴乙烷产品的制备,应用除去三颈瓶中产生的CO2、SO2,溴易挥发、有毒,为防止污染环境,应进行尾气处理,可用碱液吸收,
故答案为:防止倒吸;除去三颈瓶中产生的CO2、SO2,吸收挥发的溴蒸汽;
(5)在反应管E中进行的主要反应为乙烯和溴的加成反应,反应的方程式为:CH2=CH2+Br2→BrCH2CH2Br,
故答案为:CH2=CH2+Br2→BrCH2CH2Br;
(6)溴易挥发,为减少挥发,在反应管E中加入少量水可起到水封的作用,把反应管E置于盛有冷水的小烧杯中,可降低温度,减少挥发;
若将装置F拆除,乙烯中会混有二氧化硫,二氧化硫与溴单质反应生成硫酸和溴化氢,反应方程式为:SO2+Br2+H2O=H2SO4+2HBr,
故答案为:减少溴的挥发损失;SO2+Br2+H2O=H2SO4+2HBr.
点评:本题考查有机物制备及性质实验方案的设计,题目难度中等,解答本题的关键是把握制备实验的原理,能正确设计实验顺序,牢固把握实验基本操作时解答该类题目的保证,学习中注意加强相关知识的全面把握.

练习册系列答案
相关题目
下列化学用语正确的是( )
| A、乙酸的结构简式:C2H4O2 |
| B、氮气的结构式:N≡N |
C、硫化氢的电子式: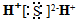 |
D、氯原子的结构示意图: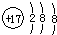 |
下列各组物质,按单质、化合物、混合物顺序排列的是( )
| A、铁、干冰、冰水混合物 |
| B、氮气、生石灰、小苏打 |
| C、液氯、烧碱、碘酒 |
| D、氯气、空气、漂粉精 |
下列有关生活生产中的叙述合理的是( )
| A、硫酸工业中SO2转化为SO3时采用常压,是因为增大压强不会提高SO2的转化率 |
| B、打开啤酒瓶的瓶盖,有大量的气泡冒出来,该现象不能用勒夏特列原理解释 |
| C、氯碱工业中用离子交换膜电解槽电解时,往阴极室注入经过精制的饱和NaCl溶液,往阳极室注入稀氢氧化钠溶液(或去离子水) |
| D、工业上合成氨采用500℃左右的温度,最主要原因是该反应的催化剂在500℃左右时活性最好 |
下列实验操作不能达到预期目的是( )
| A、用饱和NaHCO3溶液除去CO2中少量的HCl |
| B、NH4C1和I2的固体混合物可以用加热的方法分离 |
| C、植物油和水的混合物可以用分液的方法分离 |
| D、溴水中的溴单质可以用四氯化碳萃取 |