题目内容
1.用疏松多孔的活性炭插入KOH溶液作电极,在两极上分别通入甲烷和氧气,形成燃料电池,有关该电池的描述错误的是( )| A. | 电池总反应:CH4+2O2+2OH-═CO32-+3H2O | |
| B. | 负极反应式:CH4-8e-+10OH-═CO32-+7H2O | |
| C. | 正极反应式:O2+4H++4e-═2H2O | |
| D. | CH4燃料电池比CH4直接燃烧能量利用率高 |
分析 甲烷碱性燃料电池工作时,正极上投放氧气,发生得电子的还原反应,电极反应式为O2+4e-+2H2O=4OH-,甲烷在负极失电子发生氧化反应,电极反应式为CH4+10OH--8e-=CO32-+7H2O,据此解答.
解答 解:A.在碱性溶液中,负极上投放燃料甲烷,发生失电子发生氧化反应:CH4-8e-+10OH-═CO32-+7H2O,正极上投放氧气,发生得电子的还原反应:2O2+4H2O+8e-═8OH-,燃料电池的总反应式为CH4+2O2+2OH-=CO32-+3H2O,故A正确;
B.在碱性溶液中,负极上投放燃料甲烷,发生失电子发生氧化反应:CH4-8e-+10OH-═CO32-+7H2O,故B正确;
C.正极上投放氧气,发生得电子的还原反应:2O2+4H2O+8e-═8OH-,故C错误;
D.甲烷燃料电池的能量实现化学能转化为电能,能量利用率比甲烷燃烧的大,甲烷燃烧损失能量,故D正确.
故选C.
点评 本题考查了燃料电池知识,燃料电池电极反应式的书写要注意结合电解质溶液书写,原料相同,电解质溶液不同,电极反应式不同,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.在1.01×105Pa、150℃时,将 ILCH4、2LC2H2、2LC3H6与30LO2混合并点燃,完全反应后,恢复至原来状态,气体的体积是( )
| A. | 35L | B. | 30L | C. | 25L | D. | 20 L |
9.科学家于2000年合成了第116号元素(元素符号Lv).有关新质量数为293的Lv原子的描述错误的是( )
| A. | 质子数116 | B. | 中子数177 | ||
| C. | 电子数116 | D. | 该原子可表示为:${\;}_{116}^{177}$Lv |
16.下列对晶体的描述不符合科学依据的是( )
| A. | NaCl晶体中Na+和Cl-之间存在离子键,使得其熔沸点较高 | |
| B. | 金刚石晶体中碳原子以共价键方式形成了立体网状结构,熔沸点高、硬度大 | |
| C. | 足球烯分子间存在分子间作用力,其笼状结构分子使得其具有独特的性能 | |
| D. | 金属钠属于金属晶体,能导电、传热,有延展性,硬度大 |
6.Na+、Mg2+、F-、O2-四种离子具有相同的电子层结构.则四种元素原子半径由大到小的顺序分别是( )
| A. | Mg>Na>F>O | B. | O>F>Na>Mg | C. | Na>Mg>O>F | D. | O>F>Na>Mg |
13.加拿大阿尔贡天文台在星际空间发现了HC9N链状分子,其结构为:HC≡C-C≡C-C≡C-C≡C-C≡N,这是人类迄今发现的最重星际有机分子,有关该分子的说法不正确的是( )
| A. | 该物质是有机物 | B. | 该分子中含有9个σ键和10个π键 | ||
| C. | 该分子可发生加成反应 | D. | 该分子中所有原子在同一直线上 |
10.下列比较错误的是( )
| A. | 金属性:Na>Mg>Al | B. | 非金属性:Cl>S>P>Si | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 酸性:HClO>H2SO3>H3PO4>H2SiO3 |
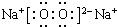 ,其中含有的化学键是离子键、共价键.
,其中含有的化学键是离子键、共价键. 现要用容量瓶配制500mL 0.4mol•L-1Na2CO3溶液,配好的溶液倒入试剂瓶后需要贴上标签.请你帮助把如图标签上的内容填上去.
现要用容量瓶配制500mL 0.4mol•L-1Na2CO3溶液,配好的溶液倒入试剂瓶后需要贴上标签.请你帮助把如图标签上的内容填上去.