题目内容
14.铜、磷及其化合物在生产、生活中有重要的用途.回答下列问题:(1)磷的一种化合物叫亚磷酸(H3PO3),已知:
Ⅰ.0.1mol/L H3PO3溶液的pH=1.7;
Ⅱ.H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ.H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3溶液有黄色沉淀生成.
①关于H3PO3的说法:a.强酸;b.弱酸;c.二元酸;d.三元酸;e.氧化性酸;f.还原性酸,其中正确的是bcf.
②写出H3PO3与少量NaOH溶液反应的离子方程式H3PO3+OH-═H2PO3-+H2O.
③Na2HPO3为正盐(填“正盐”或“酸式盐”).
(2)碘化亚铜可作催化剂、饲料添加剂等,是难溶于水的固体.铜可以与氢碘酸发生置换反应得到氢气,试从离子浓度对离子反应方向影响的角度解释此反应能够发生的原因由于CuI难溶于水,使得生成物中的离子浓度减小有利于反应向右进行,CuSO4溶液也能使淀粉-KI试纸变蓝,用离子方程式说明其原理2Cu2++4I-=2CuI↓+I2.
(3)纳米氧化亚铜是一种具有良好光电效应的材料,工业上制备它的方法之一是:先向KOH溶液中加入一定量的CuSO4溶液,再加入一定量的肼(N2H4),加热并保持反应体系的温度在90℃,反应完全后,分离、洗涤、真空干燥所得到的固体样品.检验反应混合体系内纳米Cu2O已经生成的实验方法的名称是丁达尔效应.
分析 (1)①根据酸的浓度和氢离子浓度确定酸的强弱,根据生成盐的种类确定酸的元数,根据和碘水反应P元素化合价的变化确定其氧化性、还原性;
②由H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3亚磷酸是二元酸,H3PO3与少量NaOH溶液反应生成NaH2PO3;
③亚磷酸是二元酸生成的盐Na2HPO3为正盐;
(2)碘化亚铜可作催化剂,饲料添加剂等,是难溶于水的固体.铜可以与氢碘酸发生置换反应得到氢气,是生成难溶于水的碘化亚铜促进反应正向进行,CuSO4溶液也能使淀粉-KI试纸变蓝,是铜离子氧化I-离子为I2,本身被还原生成碘化亚铜;
(3)混合体系内纳米Cu2O,氧化亚铁微粒直径符号胶体分散质微粒直径形成的分散系为胶体,检验纳米Cu2O生成,是检验溶液是否具有丁达尔效应
解答 解:(1)①由0.1mol/L H3PO3溶液的pH=1.7,说明亚磷酸部分电离,则亚磷酸是弱酸;由H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐,则说明亚磷酸是二元酸;由H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成,说明该反应中亚磷酸失电子作还原剂,所以亚磷酸有还原性,故答案为:bcf;
②由H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3亚磷酸是二元酸,H3PO3与少量NaOH溶液反应的离子方程式为:H3PO3+OH-═H2PO3-+H2O,
故答案为:H3PO3+OH-═H2PO3-+H2O;
③由H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3亚磷酸是二元酸,所以Na2HPO3为正盐,故答案为:正盐;
(2)碘化亚铜可作催化剂,饲料添加剂等,是难溶于水的固体.铜可以与氢碘酸发生置换反应得到氢气,是生成难溶于水的碘化亚铜促进反应正向进行,CuSO4溶液也能使淀粉-KI试纸变蓝,是铜离子氧化I-离子为I2,本身被还原生成碘化亚铜,结合原子守恒、电子守恒和电荷守恒配平书写离子方程式为:2Cu2++4I-=2CuI↓+I2;
故答案为:由于CuI难溶于水,使得生成物中的离子浓度减小有利于反应向右进行,2Cu2++4I-=2CuI↓+I2;
(3)纳米氧化亚铜是一种具有良好光电效应的材料,混合体系内纳米Cu2O形成胶体分散系,利用胶体的特征性质检验其存在,检验反应混合体系内纳米Cu2O已经生成的实验方法的名称是丁达尔效应,
故答案为:丁达尔效应.
点评 本题涉及物质的分类知识的考查、氧化还原反应离子方程式书写、胶体性质等知识点,注意氧化还原反应以及离子方程式的书写知识的灵活应用是关键,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 道尔顿 | B. | 牛顿 | C. | 门捷列夫 | D. | 爱迪生 |
| A. | 在常温常压下,1mol氦气含有原子数为2NA | |
| B. | 0.5molO2和0.5molO3的混合物所含有的氧原子个数为2.5NA | |
| C. | 常温常压下,2.24 LCO和CO2混合气体中含有的碳原子数目为0.1NA | |
| D. | 含NA个Na+的Na2O溶解于1 L水中,Na+的物质的量浓度为1 mol•L-1 |
| Q | X | Y | ||
| M | W | Z |
| A. | 相同条件下,Q元素最低价简单氢化物是同主族元素中氢化物沸点最高的 | |
| B. | 物质W3X4中,每个原子最外层均达到8电子稳定结构 | |
| C. | X、Q、Y和氢形成的化合物中可能既有离子键、又有共价键 | |
| D. | 将Q的最高价氧化物分别通入W的盐溶液和M的盐溶液中均可产生白色沉淀 |
I.甲组同学在进行《必修二》实验2-5“Fe3+离子在H2O2溶液分解实验中的催化作用”时,进行了以下探究.基于目前学过的元素周期表的相关知识,该小组推测了同为第四周期第VIII族的Fe、Co、Ni可能有相似的催化机理.
【查阅资料】:钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域.其中CoxNi(1-x)Fe2O4(其中Co、Ni均为+2价)也可用作H2O2分解的催化剂,具有较高的活性.
(1)写出H2O2溶液在Fe3+催化下分解的化学方程式2H2O2$\frac{\underline{\;三价铁离子\;}}{\;}$2H2O+O2↑.
(2)①该催化剂中铁元素的化合价为+3.
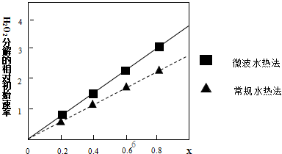
②如图表示两种不同方法制得的催化剂CoxNi(1-x)Fe2O4在10℃时催化分解6%的H2O2溶液的相对初始速率随x变化曲线.由图中信息可知:微波水热法制取得到的催化剂活性更高,由此推测Co2+、Ni2+两种离子中催化效果更好的是Co2+.
II.乙组同学在进行《选修四》实验2-2“草酸溶液浓度对酸性高锰酸钾溶液褪色时间的影响”时,发现溶液褪色总是先慢后快,该小组设计了如下过程探究其原因:
【查阅资料】KMnO4溶液氧化H2C2O4的反应历程为(流程中“III”等为Mn的价态):
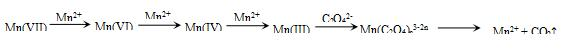
【提出假设】假设1:该反应为放热反应
假设2:反应生成的Mn2+对该反应有催化作用
假设3:K+对该反应有催化作用
【设计、完成实验】
(3)称取6.3g草酸晶体(H2C2O4•2H2O),配制500mL 0.10mol/L H2C2O4溶液.在上述过程中必须用到的2种定量仪器是托盘天平和500mL容量瓶
(4)完成探究,记录数据
| 实验 编号 | 烧杯中所加试剂及用量(mL) | 控制条件 | 溶液褪色时间(s) | |||
| 0.10 mol/L H2C2O4溶液 | 等浓度 KMnO4溶液 | H2O | 0.50 mol/L 稀硫酸 | |||
| 1 | 30 | 20 | 30 | 20 | \ | 18 |
| 2 | 30 | 20 | 30 | 20 | 水浴控制温度65℃ | 15 |
| 3 | 30 | 20 | 30 | 20 | 加入少量MnSO4固体 | 3.6 |
| 4 | 30 | 20 | x | 20 | 加入5 mL 0.10 mol/L K2SO4溶液 | 18 |
x=25mL,假设2成立(填“1”、“2”或“3”)
| 序号 | 实验内容 | 实验目的 |
| A | 在淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入少量新制的氢氧化铜悬浊液并加热 | 验证淀粉已水解 |
| B | 向2 mL甲苯中加入3滴KMnO4酸性溶液,振荡;向2mL己烷中加入3滴KMnO4酸性溶液,振荡 | 证明与苯环相连的甲基易被氧化 |
| C | 在苯酚溶液中加入溴水 | 用FeCl3溶液可检验苯酚是否完全反应 |
| D | 用苯与浓H2SO4和浓HNO3制备硝基苯,将产物倒入NaOH溶液中,静置,分液 | 除去硝基苯中混有浓H2SO4和浓HNO3 |
| A. | A | B. | B | C. | C | D. | D |
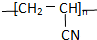 的单体正确的是( )
的单体正确的是( )| A. | 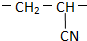 | B. | CH3-CN | C. | CH2═CHCN | D. | CH2═HCN |
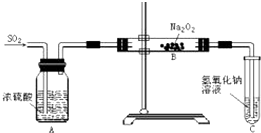 有两个实验小组的同学为探究过氧化钠与二氧化硫反应,都用如图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.
有两个实验小组的同学为探究过氧化钠与二氧化硫反应,都用如图所示的装置进行实验.通入SO2气体,将带余烬的木条插入试管C中,木条复燃.