题目内容
下表为六种短周期元素的部分性质:下列有关说法错误的是( )
| 元素代号 | X | Y | Z | Q | R | T |
| 原子半径/10-10m | 0.77 | 0.74 | 0.75 | 1.17 | 0.99 | 1.10 |
| 主要化合价 | +4、-4 | -2 | +5、-3 | +4、-4 | +7、-1 | +5、-3 |
| A、X与Y可以形成阴离子XY32- |
| B、元素R的含氧酸一定为强酸 |
| C、Z的氢化物的沸点比T的氢化物的沸点高 |
| D、由X形成的化合物QX和XR4,其晶体类型不相同 |
考点:原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:短周期元素,元素的最高正化合价与其族序数相等,最低负化合价=族序数-8,同一周期元素,原子半径随着原子序数增大而减小,同一主族元素,原子半径随着原子序数增大而增大,根据图中数据知,X和Q属于第IVA族元素、Z和I属于第VA族元素、Y属于第VIA族元素、R属于第VIIA族元素,R有正化合价所以为Cl元素,X半径小于Q,所以X为C元素、Q为Si元素;X原子半径大于Y,所以Y为O元素;Z的原子半径小于T,所以Z为N元素、T为P元素;再结合题目分析解答.
解答:
解:短周期元素,元素的最高正化合价与其族序数相等,最低负化合价=族序数-8,同一周期元素,原子半径随着原子序数增大而减小,同一主族元素,原子半径随着原子序数增大而增大,根据图中数据知,X和Q属于第IVA族元素、Z和I属于第VA族元素、Y属于第VIA族元素、R属于第VIIA族元素,R有正化合价所以为Cl元素,X半径小于Q,所以X为C元素、Q为Si元素;X原子半径大于Y,所以Y为O元素;Z的原子半径小于T,所以Z为N元素、T为P元素;
A.X与Y可以形成阴离子CO32-,故A正确;
B.R为Cl元素,其含氧酸HClO为弱酸,但为强氧化性酸,故B错误;
C.Z为N元素、T为P元素,N的氢化物中含有氢键、P的氢化物中不含氢键,氢键的存在导致氨气熔沸点高于PH3,故C正确;
D.由C形成的化合物SiC和CCl4,SiC和CCl4晶体类型分别为原子晶体、分子晶体,所以其晶体类型不同,故D正确;
故选B.
A.X与Y可以形成阴离子CO32-,故A正确;
B.R为Cl元素,其含氧酸HClO为弱酸,但为强氧化性酸,故B错误;
C.Z为N元素、T为P元素,N的氢化物中含有氢键、P的氢化物中不含氢键,氢键的存在导致氨气熔沸点高于PH3,故C正确;
D.由C形成的化合物SiC和CCl4,SiC和CCl4晶体类型分别为原子晶体、分子晶体,所以其晶体类型不同,故D正确;
故选B.
点评:本题考查原子结构和元素性质,明确元素化合价与族序数的关系、物质的结构和性质即可解答,注意Cl元素的含氧酸都具有酸性,但不一定都是强酸,为易错点.

练习册系列答案
相关题目
 已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+.现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )| A、图中AB段的氧化剂为K2Cr2O7 |
| B、图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 |
| C、开始加入的K2Cr2O7为0.25 mol |
| D、K2Cr2O7可与FeSO4反应的物质的量为1:3 |
把①pH相同的氨水和氢氧化钠溶液 ②物质的量浓度相同的醋酸和盐酸,分别加水稀释相同倍数后,pH较大的是( )
| A、①中氢氧化钠溶液较大,②中盐酸较大 |
| B、①中氨水较大,②中盐酸较大 |
| C、①中氨水较大,②中醋酸较大 |
| D、①中氢氧化钠溶液较大,②中醋酸较大 |
共价键、离子键、金属键、分子间作用力都是微粒间的作用力,含有以上两种作用力的晶体是( )
| A、HCl | B、金刚石 |
| C、NaOH | D、Na |
在pH=1的澄清透明溶液中,不能大量共存的离子组是( )
A、Al3+、Ag+、NO
| ||||
B、Cu2+、NH
| ||||
| C、Ba2+、K+、Cl-、Br- | ||||
D、Zn2+、Na+、NO
|
A、B、C、D 为4种金属.将A、B分别加入等浓度稀盐酸中,B比A反应更剧烈.将A、D用导线连结,同时浸入稀硫酸中,D表面出现大量气泡.将D浸入C的盐溶液中,有C析出.则其金属活动性由强到弱的顺序是( )
| A、B>A>D>C |
| B、A>B>D>C |
| C、B>A>C>D |
| D、C>D>A>B |
下列实验方案设计合理且能达到相应实验预期目的是( )
A、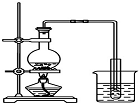 制取少量蒸馏水 |
B、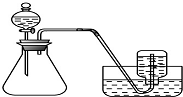 用铜和浓硝酸制取少量NO2 |
C、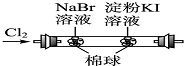 证明氧化性:Cl2>Br2>I2 |
D、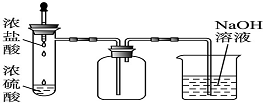 制取HCL且除去多余的气体 |
将一定量氯化钙溶于90g水中,欲使每100个水分子中含有1个Cl-,这一定量的氯化钙是( )
| A、0.3mol |
| B、0.025mol |
| C、0.05mol |
| D、5.55g |
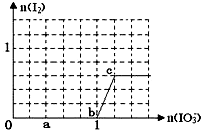 已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.在含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示,试回答下列问题:
已知溶液中:还原性HSO3->I-,氧化性IO3->I2>SO42-.在含3molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3和析出的I2的物质的量的关系曲线如右图所示,试回答下列问题: