题目内容
下列分子中,原子的最外层电子不能都满足8电子稳定结构的是( )
| A、CO2 |
| B、Cl2 |
| C、H2O |
| D、PF3 |
考点:原子核外电子排布
专题:原子组成与结构专题
分析:根据原子最外层电子数和化合价判断,在化合物中,原子最外层电子数等于原子的价层电子数+|化合价|,以此进行分析.
解答:
解:A.CO2中,C原子的最外层电子为:4+4=8,O原子的最外层电子为:6+|-2|=8,都满足8电子稳定结构,故A不选;
B.氯气分子中,Cl原子的最外层电子为:7+|-1|=8,都满足8电子稳定结构,故B不选;
C.H2O中,O原子的最外层电子数为6+2=8,H原子的最外层电子数为1+1=2,不满足8电子稳定结构,故C选;
D.PF3中,P元素的族序数+成键数=5+3=8,F为7+|-1|=8,所以该分子中所有原子最外层电子都满足8电子稳定结构,故D不选.
故选C.
B.氯气分子中,Cl原子的最外层电子为:7+|-1|=8,都满足8电子稳定结构,故B不选;
C.H2O中,O原子的最外层电子数为6+2=8,H原子的最外层电子数为1+1=2,不满足8电子稳定结构,故C选;
D.PF3中,P元素的族序数+成键数=5+3=8,F为7+|-1|=8,所以该分子中所有原子最外层电子都满足8电子稳定结构,故D不选.
故选C.
点评:本题考查了8电子稳定结构的判断,明确元素的族序数、成键数及最外层电子数即可解答,易错选项是A,注意:二氧化碳分子中,碳原子和每个氧原子形成两个共用电子对,为易错点.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
已知X、Y是主族元素,I为电离能,单位是kJ?mol-1.请根据下表所列数据判断,错误的是( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 502 | 4 600 | 6 900 | 9 500 |
| Y | 588 | 1 820 | 2 750 | 11 600 |
| A、元素X的常见化合价是+1 |
| B、若元素Y处于第3周期,它可与冷水剧烈反应 |
| C、元素Y是ⅢA族元素 |
| D、元素X与氯形成化合物时,化学式可能是XCl |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| B、在熔融状态下,lmol NaHSO4完全电离出的阳离子数为2NA |
| C、5.6 g铁粉在2.24L(标准状况)氯气中充分燃烧,失去的电子数为0.3NA |
| D、78g Na2O2固体与H2O完全反应转移的电子数为NA |
 钙、铝、铜都是中学化学中常见的金属元素.
钙、铝、铜都是中学化学中常见的金属元素.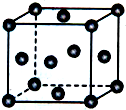 已知X、Y、Z为短周期元素,X、Y同周期,X和Z同主族,Y原子基态时2p轨道上的未成对电子数最多,X的低价氧化物和Y单质分子的电子数相等.W2+的核外电子排布简式为[Ar]3d9.
已知X、Y、Z为短周期元素,X、Y同周期,X和Z同主族,Y原子基态时2p轨道上的未成对电子数最多,X的低价氧化物和Y单质分子的电子数相等.W2+的核外电子排布简式为[Ar]3d9.