题目内容
3.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是①CH3OH(g)+H2O(g)═CO2(g)+3H2(g);△H=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g);△H=-192.9kJ•mol-1
下列说法正确的是( )
| A. | CH3OH的燃烧热为192.9kJ•mol-1 | |
| B. | CH3OH转变成H2的过程一定要吸收能量 | |
| C. | 可推知2H2(g)+O2(g)═2H2O(g)△H=-483.8 kJ/mol | |
| D. | 根据②推知反应:CH3OH(l)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)的△H<-192.9kJ•mol-1 |
分析 A、利用盖斯定律,②×3-①×2可得甲醇燃烧的热化学方程式,进而可知甲醇的燃烧热;
B、根据△H=生成物总能量-反应物总能量来判断;
C、根据物质的能量大小与物质的状态关系来判断;
D、根据物质的能量大小与物质的状态关系来判断.
解答 解:A、根据盖斯定律将,②×3-①×2可得:CH3OH(g)+$\frac{3}{2}$O2(g)=CO2(g)+2H2O(l)△H=-192.9kJ/mol×3-49kJ/mol×2=-676.7kJ/mol,所以甲醇的燃烧热为676.7kJ/mol,故A错误;
B、反应①的△H>0,而图示的△H=生成物总能量-反应物总能量<0,故B错误;
C、同物质的量的同种物质,气态能量最高,其次液态能量,固态能量最低,由②推知反应:CH3OH(l)+$\frac{1}{2}$O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ•mol-1,故C正确;
D、同物质的量的同种物质,气态能量最高,其次液态能量,固态能量最低,由②推知反应:CH3OH(l)+$\frac{1}{2}$O2(g)=CO2(g)+2H2(g)的△H>-192.9kJ•mol-1,故D错误;
故选C.
点评 本题考查化学反应的反应热的计算.注意在比较反应热大小时要带符号比较,并注意盖斯定律的应用来解答.

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
13.几种短周期元素的原子半径及主要化合价如表( )
下列叙述错误的是(其中NA表示阿伏加德罗常数的值)
| 元素代号 | X | Y | Z | M | N | P |
| 原子半径/nm | 0.186 | 0.143 | 0.075 | 0.074 | 0.152 | 0.099 |
| 元素的主要化合价 | +1 | +3 | +5、-3 | -2 | +1 | +7、-1 |
| A. | X、N元素的金属性:X>N | |
| B. | Y、M元素形成的离子化合物是工业冶炼Y的原料 | |
| C. | X单质在M单质中燃烧生成的化合物39g中共含有0.5NA个阴离子 | |
| D. | 表中Z元素的最高价氧化物的水化物的分子式可表示为H3ZO4 |
14.能源可分为一级能源和二级能源.下列叙述正确的是( )
| A. | 水煤气是一级能源 | B. | 天然气是二级能源 | ||
| C. | 电能是二级能源 | D. | 水力是二级能源 |
11.X、Y是元素周期表第VIIA族的两种元素,下列说法中能说明X的非金属性比Y强的是( )
| A. | X元素原子的电子层数比Y元素原子的电子层数多 | |
| B. | X的气态氢化物比Y的气态氢化物稳定 | |
| C. | X的最高价氧化物对应水化物的酸性比Y的弱 | |
| D. | Y的单质能将X从NaX溶液中置换出来 |
18.在通常条件下,下列各组物质的性质排列不正确的是( )
| A. | 还原性强弱:CI-<Br一<I - | B. | 微粒半径大小:S>Na+>O2- | ||
| C. | 热稳定性:HF>H2O>NH3 | D. | 碱性:KOH>NaOH>LiOH |
8.下列实验能获得成功的是( )
| A. | 制取溴苯:铁屑、溴水、苯 | |
| B. | 要检验卤代烃中的卤素原子,可向其溶液中加入AgNO3溶液 | |
| C. | 苯酚有酸性,可使紫色石蕊变红 | |
| D. | 用溴水可鉴别苯、CCl4、苯乙烯 |
12.下列关于粒子结构的描述不正确的是( )
| A. | H2S和NH3均是价电子总数为8的分子 | |
| B. | HS-和HCl均是含一个极性键的18电子粒子 | |
| C. | CO2的电子式为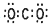 | |
| D. | 1 mol D216O中含中子、质子、电子各10 NA(NA代表阿伏加德罗常数的值) |
13.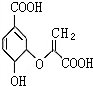 分支酸在植物的芳香族氨基酸的合成系统中作为中间体,其结构简式如图.下列关于分支酸的叙述正确的是( )
分支酸在植物的芳香族氨基酸的合成系统中作为中间体,其结构简式如图.下列关于分支酸的叙述正确的是( )
 分支酸在植物的芳香族氨基酸的合成系统中作为中间体,其结构简式如图.下列关于分支酸的叙述正确的是( )
分支酸在植物的芳香族氨基酸的合成系统中作为中间体,其结构简式如图.下列关于分支酸的叙述正确的是( )| A. | 分支酸属于芳香族化合物 | |
| B. | 遇氯化铁溶液发生显色反应,可用于检验分支酸 | |
| C. | 1 mol分支酸最多可与3molH2发生加成反应 | |
| D. | 1 mol分支酸与足量NaHCO3溶液反应放出67.2L二氧化碳气体 |
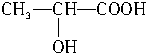
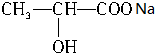 +CO2↑+H2O
+CO2↑+H2O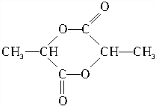 +2H2O.
+2H2O.