题目内容
15.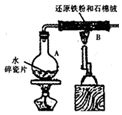 某校化学小组学生利用如图所示装置进行“铁与水反应”的实验,并探究固体产物成分(图中夹持及尾气处理装置均已略去).
某校化学小组学生利用如图所示装置进行“铁与水反应”的实验,并探究固体产物成分(图中夹持及尾气处理装置均已略去).Ⅰ.装置B中发生反应的化学方程式是3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2;
Ⅱ.停止反应后,待B管冷却,称量,再向固体中加入过量稀盐酸充分反应,并进行如下实验:

(1)试剂a的化学式是KSCN,试剂b的化学式是NaOH;
(2)加入新制氯水后溶液红色加深的原因是(用离子方程式表示)2Fe2++Cl2=2Fe3++2Cl-;
(3)某同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现请对褪色原因进行探究:
①提出假设:假设1:溶液中的+3价铁被氧化为更高的价态;
假设2:SCN-被过量的氯水氧化;
②设计方案:为了对所提出的假设2进行验证,实验方案是取少量褪色后的溶液,滴加过量KSCN溶液,如果出现红色,则说明假设2正确,若不变红,则假设2不正确.
分析 I.(1)装置B中,水蒸气和铁粉高温下发生氧化还原反应,生成Fe3O4和氢气;
II.得到固体质量为28.8g,加入过量稀盐酸充分反应,得到浅黄色溶液,应为FeCl3,加入试剂a变为淡红色,则加入的试剂为KSCN,加入新制备氯水,溶液颜色加深,说明Fe3+浓度增大,Fe2+被氯水氧化生成Fe3+,然后加入氢氧化钠溶液,可得到氢氧化铁固体,经过滤、加强热,可分解生成红棕色氧化铁固体;
可取少量褪色后的溶液,再滴加过量KSCN溶液,如果出现红色,说明被KSCN氧化,反之+3价铁被氧化;
解答 解:I.装置B中,水蒸气和铁粉高温下发生氧化还原反应,生成Fe3O4和氢气,方程式为3Fe+4H2O(g) $\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2,
故答案为:3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+4H2;
Ⅱ.(1)得到固体质量为28.8g,加入过量稀盐酸充分反应,得到浅黄色溶液,应为FeCl3,加入试剂a变为淡红色,则加入的试剂为KSCN,加入新制备氯水,溶液颜色加深,说明Fe3+浓度增大,Fe2+被氯水氧化生成Fe3+,然后加入氢氧化钠溶液,可得到氢氧化铁固体,经过滤、加强热,可分解生成红棕色氧化铁固体,
故答案为:KSCN;NaOH;
(2)加入新制氯水后溶液红色加深的原因是亚铁离子被氧化,方程式为2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(3)①某同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,可能原因是+3价铁被氧化或SCN-被过量的氯水氧化,
故答案为:SCN-被过量的氯水氧化;
②为了对所提出的假设2进行验证,实验方案是可取少量褪色后的溶液,再滴加过量KSCN溶液,如果出现红色,说明被KSCN氧化,反之+3价铁被氧化,
故答案为:取少量褪色后的溶液,滴加过量KSCN 溶液,如果出现红色,则说明假设2 正确,若不变红,则假设2 不正确.
点评 本题考查物质的含量测定以及性质实验方案的设计,为高考常见题型,题目以铁以及其化合物的相互转化为载体,侧重于实验方案设计与评价,题目难度中等,注意把握实验原理和实验目的.

 通城学典默写能手系列答案
通城学典默写能手系列答案| A. | 124 g P4含有P-P键的个数为4NA | |
| B. | 60gSiO2中含Si-O键的个数为2NA | |
| C. | 12 g石墨中含有C-C键的个数为1.5NA | |
| D. | 36 g戊烷中共价键的个数为10NA |
| A. | $\frac{1}{14}$ mol•L-1 | B. | $\frac{4}{5}$ mol•L-1 | C. | $\frac{1}{28}$ mol•L-1 | D. | $\frac{1}{42}$ mol•L-1 |
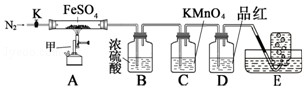
查阅资料得知:SO3溶于水会形成大量的酸雾,工业上通常用浓硫酸做为SO3吸收剂.
实验步骤:按图组装好仪器(已省略夹持仪器)并检查装置的气密性,准确称取m g FeSO4固体置于硬质玻璃管中,将E中的导管撤出水槽,打开活塞K,通入一段时间的N2,关闭活塞K.加热A中的玻璃管一段时间后,将E中导管置于水槽集气瓶口收集产生的气体,用带火星的木条检验E中所收集的气体,带火星的木条能够复燃.待A中固体不再分解后,停止加热,打开K,缓慢通入氮气至玻璃管冷却,得到红棕色粉末.请回答下列问题:
(1)B中浓硫酸的作用是吸收分解产生的SO3;
(2)实验前通入一段时间N2,目的是排尽装置中的空气;FeSO4完全分解后,还需要通入一段时间N2,原因是将装置内残留的气体排入吸收装置,使其完全被吸收;
(3)实验过程中发现C中溶液颜色变浅,D中无明显变化.写出C中发生反应的离子方程式5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+;
| 实验 | 滴定管 开始读数 | 滴定 终点读数 |
| 1 | 0 | 19.98 |
| 2 | 0.10 | 20.12 |
| 3 | 0 | 20.16 |
I、称量B装置在实验前后增重0.80g;
II、将实验后C中的溶液全部转移至100mL容量瓶中,并加水稀释至刻度线;
III、准确量取20.00mL溶液至锥形瓶中,加入足量稀硫酸酸化,用0.20mol/L标准H2C2O4溶液滴定至终点;
IV、重复实验3次,记录数据如表
①滴定至终点的现象溶液由紫红色变为无色且半分钟不恢复成紫红色;
②FeSO4分解的化学方程式为8FeSO4$\frac{\underline{\;高温\;}}{\;}$4Fe2O3+2SO3↑+6SO2↑+O2↑;
(5)请设计一个实验来检验A中的FeSO4是否完全分解将废液后的固体转移到小烧杯中,加入少量水搅拌过滤,取少量滤液于试管中,加入几滴K3[Fe(CN)6]溶液,若产生特征蓝色沉淀,说明硫酸亚铁未全部分解,反之则分解完全.
| 元素 | 相 关 信 息 |
| A | 原子核外有7种运动状态不同的电子 |
| B | 外围电子排布式为nsnnpn+2 |
| C | 常见的金属,在周期表中周期序数与族序数相等 |
| D | 气态氢化物及最高价氧化物对应的水化物均为强酸 |
| E | 一种核素的质量数为56,中子数为30 |
| F | 单质紫红色,电缆材料,常见氧化物为黑色 |
(1)元素E在元素周期表中的位于第四周期第Ⅷ族,其高价态离子核外有5个未成对电子
(2)B、C、D三种元素的离子半径由小到大的顺序是r(Al3+)<r(O2-)<r(C1-)(用离子符号表示).
(3)A、D两元素的简单氢化物发生反应生成的化合物的电子式为
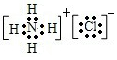
(4)常温下AD3是一种淡黄色液体.以下关于AD3的说法中,正确的是BC
A.AD3分子中只有非极性键 B.AD3分子中各原子均达8e-稳定结构
C.AD3的晶体属于分子晶体 D.AD3液体气化时化学键被破坏
(5)金属C与E的黑色磁性晶体氧化物在高温下反应,该反应的化学方程式为3Fe3O4+8Al$\frac{\underline{\;高温\;}}{\;}$9Fe+4Al2O3
(6)向F的硫酸盐溶液中通入AH3气体至过量,观察到的现象是蓝色溶液先产生蓝色沉淀,最后沉淀溶解,形成深蓝色溶液;该过程总的离子反应式为Cu2++4NH3=[Cu(NH3)4]2+或Cu2++4 NH3•H2O=[Cu(NH3)4]2++4H2O向反应后的溶液中加入适量乙醇,析出深蓝色晶体,该晶体中不含有的化学键类型是C
A.配位键 B.极性共价键 C.非极性共价键 D.离子键.
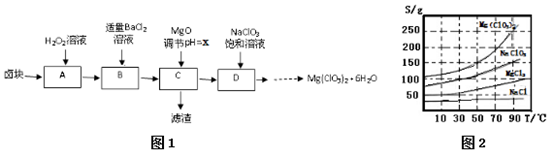
已知:①四种化合物的溶解度(S)随温度(T)变化曲线如图2所示.
②室温时一些物质的Ksp如表:
| 化学式 | Fe(OH)2 | Fe(OH)3 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 8.0×10-38 | 1.8x10-11 |
(1)H2O2的电子式为
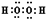
(2)滤渣的成分是Fe(OH)3、BaSO4(填化学式);
(3)经测定,D中铁离子的浓度为1×10-5 mol/L,则x为3.3
(4)D中所发生的化学反应方程式式为MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,框图中由D→…→制Mg(ClO3)2•6H2O晶体的实验步骤依次为:①加热蒸发;②趁热过滤(请补充);③冷却结晶;④过滤洗涤.
(5)产品中Mg(ClO3)2•6H2O含量的测定:
步骤1:准确称量3.50g产品配成100mL溶液.
步骤2:取10.00mL试液于锥形瓶中,加入10.00mL稀硫酸和20.00mL 1.000mol/L的FeSO4溶液,微热.
步骤3:冷却至室温,用0.100mol/L K2Cr2O7溶液滴定剩余的Fe2+至终点.
步骤4:将步骤2、3重复两次
①步骤3中发生反应的离子方程式Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O
②步骤3中若滴定前不用标准液润洗滴定管,将会导致最终结果偏小(填“偏大”.“偏小”或“不变”).
③若平均消耗K2Cr2O7溶液15.00mL,则产品中Mg(ClO3)2•6H2O(其M=299g/mol)的质量分数为78.3%.
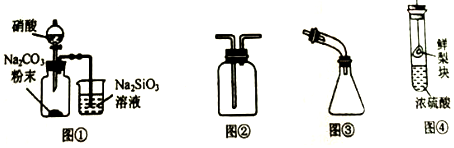
| A. | 图①:证明非金属性由强到弱的顺序是N>C>Si | |
| B. | 图②:收集NO2或NH3 | |
| C. | 图③:海水蒸馏时接收蒸馏水 | |
| D. | 图④:探究浓硫酸的脱水性 |