题目内容
( 9分)重铬酸钾(K2Cr2O7)是重要氧化剂,重铬酸钾的溶解度受温度影响较大,工业上常用铬铁矿(主要成分为FeO?Cr2O3,杂质为SiO2?Al2O3)为原料生产它。实验室模拟工业上用铬铁矿制 K2CrO7的主要工艺流程如下图。涉及“碱熔”的主要反应为:
6 FeO?Cr2O3 + 24NaOH + 7KC1O3 = 12NaCrO4 + 3Fe2O3 + 7KCl + 12H2O
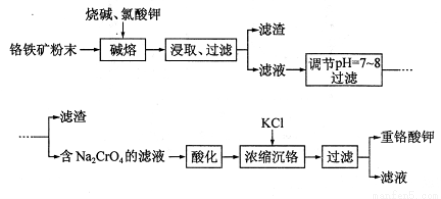
(1)使用粉末状铬铁矿的目的是 。
(2)调节pH后,过滤得到的滤渣是 (填化学式)。
(3)酸化Na2CrO4溶液时,其平衡转化的离子方程式为 。
(4)称取重铬酸钾试样2.500g配成500mL溶液,取出25.00mL于锥形瓶中,加入10 mL2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入100 mL 水,加人3mL淀粉溶液(作指示剂),用0.1200 mol/LNa2S2O3标准溶液滴定( I2 + 2S2O2- 3= 2I-+S4O2- 6),用去20.00mL ,则该样品的纯度为 。
(1)增大接触面积,加快化学反应速率,且使铬铁矿充分反应;(2)Al(OH)3、H2SiO3;
(3)2CrO42-+2H+ Cr2O72-+H2O;(4)0.9408.
Cr2O72-+H2O;(4)0.9408.
【解析】
试题分析:(1)使用粉末状铬铁矿的目的是增大接触面积,加快化学反应速率,且使铬铁矿充分反应;(2)铬铁矿用烧碱、氯酸钾溶解后得到的物质中,难溶性的固体物质有Fe2O3;滤液中含有NaCrO4 、KCl、NaAlO2、Na2SiO3;当调节pH为7~8后,Al、Si就形成Al(OH)3、H2SiO3沉淀经过过滤除去,而在滤液中含有NaCrO4 、KCl;(3)酸化Na2CrO4溶液时,其平衡转化的离子方程式为2CrO42-+2H+ Cr2O72-+H2O;(4)根据电子守恒可得:Cr2O72-~3 I2 ~ 6S2O2- 3;n(S2O32-)= 0.1200 mol/L×0.020L=2.4×10-3mol;所以在25.00mL重铬酸钾试样中含有溶质的物质的量是4×10-4mol,所以重铬酸钾试样2.500g配成500mL溶液中含有溶质的物质的量是(500mL÷25.00mL)×4×10-4mol=8×10-3mol.n(K2Cr2O7)= 8×10-3mol×294g/mol=2.352g,所以该样品的纯度为(2.352g÷2.500g)×100%=94.8%。
Cr2O72-+H2O;(4)根据电子守恒可得:Cr2O72-~3 I2 ~ 6S2O2- 3;n(S2O32-)= 0.1200 mol/L×0.020L=2.4×10-3mol;所以在25.00mL重铬酸钾试样中含有溶质的物质的量是4×10-4mol,所以重铬酸钾试样2.500g配成500mL溶液中含有溶质的物质的量是(500mL÷25.00mL)×4×10-4mol=8×10-3mol.n(K2Cr2O7)= 8×10-3mol×294g/mol=2.352g,所以该样品的纯度为(2.352g÷2.500g)×100%=94.8%。
考点:考查影响化学反应速率的因素、反应条件的选择、守恒法在化学计算中的应用、物质纯度的计算的知识。

 全优点练单元计划系列答案
全优点练单元计划系列答案
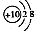 B.Na2S的电子式:
B.Na2S的电子式: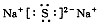
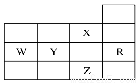
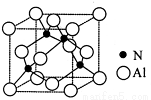
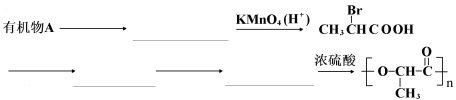
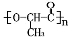 是一种很有前途的可降解高分子材料,可制成袋子替代日常生活中的大部分塑料袋。请完成以有机物A为原料合成聚乳酸的路线(无机试剂任选)
是一种很有前途的可降解高分子材料,可制成袋子替代日常生活中的大部分塑料袋。请完成以有机物A为原料合成聚乳酸的路线(无机试剂任选)