题目内容
25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A、pH=1的溶液中:Na+、K+、MnO4-、CO32-、 |
| B、c(H+)=1×10-13 mol?L-1的溶液中:Mg2+、Cu2+、NO3- |
| C、0.1 mol?L-1NH4HCO3溶液中:K+、Na+、NO3-、Cl- |
| D、0.1 mol?L-1FeCl3溶液中:Fe2+、SCN-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:A.pH=1的溶液,显酸性;
B.c(H+)=1×10-13 mol?L-1的溶液,显碱性;
C.该组离子之间不反应;
D.离子之间结合生成络离子.
B.c(H+)=1×10-13 mol?L-1的溶液,显碱性;
C.该组离子之间不反应;
D.离子之间结合生成络离子.
解答:
解:A.pH=1的溶液,显酸性,H+、CO32-结合生成水和气体,不能大量共存,故A错误;
B.c(H+)=1×10-13 mol?L-1的溶液,显碱性,不能大量存在Mg2+、Cu2+,故B错误;
C.该组离子之间不反应,能大量共存,故C正确;
D.Fe3+、SCN-离子之间结合生成络离子,不能大量共存,故D错误;
故选C.
B.c(H+)=1×10-13 mol?L-1的溶液,显碱性,不能大量存在Mg2+、Cu2+,故B错误;
C.该组离子之间不反应,能大量共存,故C正确;
D.Fe3+、SCN-离子之间结合生成络离子,不能大量共存,故D错误;
故选C.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、络合反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
用NaOH固体配制1mol/L的NaOH溶液500ml,下列操作和说法中正确的是( )
| A、称量时,将固体NaOH直接放在天平左盘上 |
| B、将烧杯中溶解固体NaOH所得溶液,立即转移至500ml容量瓶中 |
| C、配制溶液时容量瓶中原来有少量蒸馏水不会影响实验结果 |
| D、缓缓地将蒸馏水注入500ml容量瓶至溶液的凹液面正好与刻度线相切 |
以化学平衡与化学反应速率的关系可知( )
| A、化学反应速率变化时,化学平衡一定发生移动 |
| B、化学平衡发生移动时、化学反应速率一定变化 |
| C、正反应进行的程度大、正反应速率一定大 |
| D、只有使用催化剂才会发生化学反应速率变化,而化学平衡不移动的情况. |
下列说法不正确的是( )
| A、陶瓷是以黏土和石灰石为原料,经高温烧结而成的 |
| B、高纯单质硅可以制成光电池,将光能直接转换为电能 |
| C、水玻璃可作木材的防火剂 |
| D、向饱和Na2SiO3溶液中通入足量CO2,然后蒸发结晶,最后灼烧,得到Na2CO3、SiO2 |
下列说法正确的是( )
| A、非自发进行的反应一定不能发生 |
| B、自发进行的反应一定能迅速发生 |
| C、在一定条件下,非自发进行的反应也能发生 |
| D、吸热反应一定不能自发进行 |
下列各组为两种元素的原子序数,其中不能反应生成AB3型化合物的是( )
| A、13和17 | B、16和8 |
| C、9和11 | D、7和1 |
下列说法正确的是( )
| A、氢键、分子间作用力、离子键、共价键都是微粒间的作用力.其中分子间作用力只影响物质的熔沸点而不影响物质的溶解性 |
| B、石墨烯是一种从石墨材料中用“撕裂”方法剥离出的单层碳原子面材料,用这种方法从C60、金刚石等中获得“只有一层碳原子厚的碳薄片”也必将成为研究方向 |
| C、结合质子能力由强到弱的顺序是OH->CH3COO->Cl- |
D、原子结构模型的演变经历了: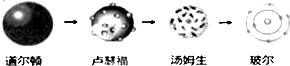 |
如图所示2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是( )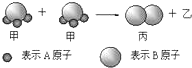

| A、根据阿伏加德罗定律可推知,1个乙分子中含有2个A原子 |
| B、该反应类型是分解反应 |
| C、该反应一定属于氧化还原反应 |
| D、Mr(甲)=Mr(乙)+Mr(丙) |