题目内容
某原子核内的质子数为m,中子数为n,则下述论断正确的是( )
| A、原子核内中子的总质量小于质子的总质量 |
| B、该原子的质量数等于m-n |
| C、该元素的相对原子质量近似等于m+n |
| D、该原子的相对原子质量近似等于m+n |
考点:质量数与质子数、中子数之间的相互关系
专题:原子组成与结构专题
分析:A、质子数和中子数的相对多少未知,无法判断;
B、质量数=质子数+中子数;
C、无法计算该元素的相对原子质量;
D、电子的质量很小,原子的相对原子质量近似等于质量数.
B、质量数=质子数+中子数;
C、无法计算该元素的相对原子质量;
D、电子的质量很小,原子的相对原子质量近似等于质量数.
解答:
解:A、一个质子的质量和一个中子的质量相当,质子数和中子数的相对多少未知,导致无法判断,故A错误;
B、该原子的质量数=质子数+中子数=m+n,故B错误;
C、题目已知某元素的一种核素的质子数和中子数,该核素的丰度未知导致无法计算该元素的相对原子质量,故C错误;
D、由于电子的质量很小,原子的相对原子质量近似等于质子数+中子数,故D正确;
故选D.
B、该原子的质量数=质子数+中子数=m+n,故B错误;
C、题目已知某元素的一种核素的质子数和中子数,该核素的丰度未知导致无法计算该元素的相对原子质量,故C错误;
D、由于电子的质量很小,原子的相对原子质量近似等于质子数+中子数,故D正确;
故选D.
点评:本题考查了元素的相对原子质量的计算、核素的相对原子质量的计算等知识点,难度不大,明确元素和核素的相对原子质量的计算方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法正确的是( )
| A、需要加热的化学反应都是吸热反应 |
| B、物质的燃烧都是放热反应 |
| C、原电池是将电能转化为化学能的一种装置 |
| D、水力发电是将化学能转化为电能的过程 |
下列有关FeCl3溶液和Fe(OH)3胶体叙述正确的是( )
| A、向FeCl3溶液和Fe(OH)3胶体中加入饱和NaCl溶液都不产生沉淀 |
| B、用滤纸过滤分离FeCl3溶液和Fe(OH)3胶体的混合物 |
| C、FeCl3饱和溶液与NaOH浓溶液混合即可制备得到Fe(OH)3胶体 |
| D、向Fe(OH)3胶体中逐滴滴入盐酸先产生沉淀,后沉淀溶解 |
在容积为2L的密闭容器中充入2mol SO2和一定量O2,发生反应2SO2+O2?2SO3,当反应进行到4min时,测得n(SO2)=0.6mol.若反应进行到2min时,容器中SO2的物质的量是( )
| A、等于1.3mol |
| B、小于1.3mol |
| C、大于1.4mol |
| D、等于1.4mol |
在同温同压下,等体积的CO2和CO一定具有:①相同的质量 ②相同的密度 ③相同的分子数 ④相同的碳原子数( )
| A、①② | B、②③ | C、③④ | D、④ |
下列文字表述与反应方程式对应不正确的是( )
A、甲烷和氯气取代:CH4+Cl2
| |||
B、乙烯和水加成:CH2=CH2+H2O
| |||
C、苯酚钠溶液中通少量CO2:CO2+H2O+ → →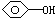 +HCO3- +HCO3- | |||
D、实验室用液溴和苯在催化剂作用下制溴苯: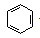 +Br2 +Br2
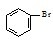 +HBr +HBr |
设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
| A、1mol NH3所含有的原子数为NA |
| B、常温常压下,22.4L氧气所含的原子数为2NA |
| C、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
| D、1L 0.1mol/L NaCl溶液中所含的Na+为NA |
下列叙述正确的是( )
| A、P4和CO2分子中都只含有共价键 |
| B、CCl4和NH3的分子的立体结构都是正四面体形 |
| C、BF3分子中各原子均达到8e-稳定结构 |
D、甲烷的结构式为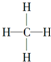 ,它是对称的平面形分子 ,它是对称的平面形分子 |