题目内容
|
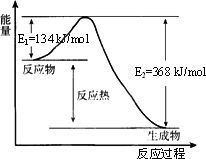
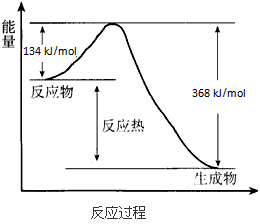
在400℃、101 kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如下图所示.下列说法不正确的是
| |
| [ ] | |
A. |
该反应是放热反应 |
B. |
该反应的反应热ΔH=-234 kJ/mol |
C. |
加入催化剂,使该反应的活化能降低,反应速率加快,同时使该反应的反应热数值减小 |
D. |
由图可推出:NO(g)+CO2(g) |
答案:C

练习册系列答案
相关题目
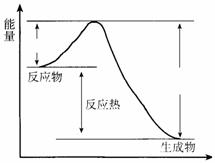
在400 ℃、101 kPa时,NO2(g)+CO(g) NO(g) + CO2(g)反应过程的能量变化如下图所示。
反应过程
(1)该反应是 (填“吸热”或“放热”)反应。
(2)该反应的热化学方程式为 。
(3)改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的是 (填序号)。
a.浓度 | b.压强 |
c.温度 | d.催化剂 |