题目内容
已知:氯气与一定浓度的氢氧化钠反应生成次氯酸与氯酸钠之比为1:2,
(1)写出该反应的化学方程式: ;
(2)求被氧化与被还原的氯气的质量之比: ;
(3)参加反应的氯气与氢氧化钠物质的量之比: .
(1)写出该反应的化学方程式:
(2)求被氧化与被还原的氯气的质量之比:
(3)参加反应的氯气与氢氧化钠物质的量之比:
考点:氧化还原反应的计算,化学方程式的有关计算
专题:
分析:生成次氯酸与氯酸钠之比为1:2,结合电子守恒可知还生成NaCl,结合电子、原子守恒可知反应为7Cl2+14NaOH═11NaCl+NaClO+2NaClO3+7H2O,11个Cl原子被还原,同时3个Cl原子被还原,以此来解答.
解答:
解:(1)生成次氯酸与氯酸钠之比为1:2,失去电子数为11,则还生成NaCl得到电子,得电子数应为11,即由电子、原子守恒可知反应为7Cl2+14NaOH═11NaCl+NaClO+2NaClO3+7H2O,
故答案为:7Cl2+14NaOH═11NaCl+NaClO+2NaClO3+7H2O;
(2)由反应可知,11个Cl原子被还原,同时3个Cl原子被还原,则被氧化与被还原的氯气的质量之比为3:11,故答案为:3:11;
(3)由反应可知,氯气与NaOH以7:11的物质的量比反应,故答案为:7:11.
故答案为:7Cl2+14NaOH═11NaCl+NaClO+2NaClO3+7H2O;
(2)由反应可知,11个Cl原子被还原,同时3个Cl原子被还原,则被氧化与被还原的氯气的质量之比为3:11,故答案为:3:11;
(3)由反应可知,氯气与NaOH以7:11的物质的量比反应,故答案为:7:11.
点评:本题考查氧化还原反应的计算,为高频考点,把握电子守恒、原子守恒确定氧化还原反应为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
2.1g平均相对分子质量为7.2的CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足量的Na2O2固体中,固体的质量增加( )
| A、2.1g | B、3.6g |
| C、7.2g | D、无法确定 |
下列离子方程式书写正确的是( )
| A、往NaOH溶液中通入少量CO2:CO2+OH-═HCO3- |
| B、单质Si与氢氟酸反应:Si+4HF═H2↑+SiF4↑ |
| C、石英砂与烧碱反应制水玻璃:SiO2+2OH-═SiO32-+H2O |
| D、往水玻璃中通入二氧化碳:Na2SiO3+H2O+CO2═H2SiO3↓+2Na++CO32- |
NO、NO2可被氨水溶液吸收(6NO+4NH3→5N2+6H2O;6NO2+8NH3→7N2+12H2O).现有NO与NO2(不含N2O4)混合气体90mol被30%的氨水4.45×103g完全吸收,产生78mol氮气.吸收后氨水密度为0.980g/cm3.则( )
| A、原混合气体的平均组成为NO1.1 |
| B、原氨水的浓度约为17.3mol/L |
| C、吸收后氨水的浓度约为2.4mol/L |
| D、吸收后氨水的质量分数约为0.5 |
 pH=11的X、Y两种碱溶液各5mL,分别稀释至500mL,其pH随溶液体积(V)变化的关系如图所示,下列说法正确的是( )
pH=11的X、Y两种碱溶液各5mL,分别稀释至500mL,其pH随溶液体积(V)变化的关系如图所示,下列说法正确的是( )| A、稀释后X溶液中水的电离程度比Y溶液中水的电离程度小 |
| B、若X、Y是一元碱,等物质的量浓度的盐酸盐溶液,Y的pH大 |
| C、完全中和X、Y两溶液时,消耗同浓度稀硫酸的体积:V(X)>V(Y) |
| D、若X、Y都是一元弱碱,则a的值一定大于9 |
 目前工业上有一种用CO2来生产燃料甲醇的方法,可以将CO2变废为宝.
目前工业上有一种用CO2来生产燃料甲醇的方法,可以将CO2变废为宝.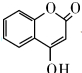 可用制备抗凝血药,通过下列路线合成:
可用制备抗凝血药,通过下列路线合成:
