题目内容
4.对于硫酸工业中SO2的催化氧化反应 2SO2+O2$?_{△}^{催化剂}$2SO3,下列说法错误的是( )| A. | 使用催化剂能加快化学反应速率 | |
| B. | 增大O2浓度可以使SO2转化率达到100% | |
| C. | 降低反应温度,化学反应速率减慢 | |
| D. | 增大O2浓度,化学反应速率增大 |
分析 A、催化剂降低反应活化能增大反应速率;
B、增大氧气浓度增大二氧化硫转化率,但反应是可逆反应最后达到平衡状态;
C、降低温度反应速率减小;
D、增大反应物浓度,反应速率增大.
解答 解;A、催化剂降低反应活化能增大反应速率,使用催化剂能显著增大反应速率,故A正确;
B、增大氧气浓度,增大二氧化硫转化率,氧气转化率减小,反应是可逆反应最后达到平衡状态时,不能反应完全,二氧化硫转化率不能达到100%,故B错误;
C、降低反应温度,正逆反应速率都减小,化学反应速率减慢,故C正确;
D、增大反应物浓度,反应速率增大,增大O2浓度可以增大反应速率,故D正确;
故选B.
点评 本题考查了化学平衡影响因素分析判断,反应速率的影响因素分析判断,掌握基础是解题关键,题目较简单.

练习册系列答案
相关题目
11.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 7.8 g Na2O2与足量H2O反应,电子转移1.204×1023 NA个 | |
| B. | 16 g O2和O3的混合气体中,含O原子 NA个 | |
| C. | 1.12 L氯气中含有0.1 NA个氯原子 | |
| D. | 标准状况下,2.24 L水中含有0.1 NA个水分子 |
19.A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族.B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物.
请回答下列问题:
(1)C、D、E三种原子对应的离子半径由大到小的顺序是S2->O2->Na+(填离子符号)
(2)A、B、C、D的任意三种元素可组成多种化合物,X和Y是其中的两种;X和Y都是既含离子键又含有共价键的离子化合物:将X、Y分别溶于水时,X能促进水的电离,而Y能抑制水的电离,X水溶液的PH<7,Y水溶液PH>7.将0.2mol/L的X溶液与0.1mol/L的Y溶液等体积混合后,溶液呈碱性.请判断:
①X的化学式为NH4NO3,Y的化学式为NaOH
②混合溶液中各种带电微粒的物质的量的浓度由大到小的顺序为c(NO3-)>c(NH4+)>c(Na+ )>c(OH-)>c(H+)
(3)A、C两元素的单质与熔融K2CO3组成的燃料电池,其负极反应式为H2+CO32--2e-=CO2↑+H2O用该电池电解1L 1mol/L NaCl溶液,当消耗标准状况下1.12L A2时,NaCl溶液的PH=13(假设电解过程中溶液的体积不变).
(4)25℃,两种酸的电离平衡常数如下表:
请写出H2SO3溶液和NaHCO3溶液反应的主要离子方程式H2SO3+HCO3-=HSO3-+H2O+CO2↑
(5)常温下0.2mol/L的H2C2O4溶液的PH为2.1.H2C2O4与酸性高锰酸钾溶液反应,现象是有气泡(CO2)产生,紫红色消失.写出反应的离子方程式2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O又知该反应开始时速率较慢,随后大大加快,可能的原因是反应生成Mn2+对反应起到催化作用(忽略反应的热效应)
请回答下列问题:
(1)C、D、E三种原子对应的离子半径由大到小的顺序是S2->O2->Na+(填离子符号)
(2)A、B、C、D的任意三种元素可组成多种化合物,X和Y是其中的两种;X和Y都是既含离子键又含有共价键的离子化合物:将X、Y分别溶于水时,X能促进水的电离,而Y能抑制水的电离,X水溶液的PH<7,Y水溶液PH>7.将0.2mol/L的X溶液与0.1mol/L的Y溶液等体积混合后,溶液呈碱性.请判断:
①X的化学式为NH4NO3,Y的化学式为NaOH
②混合溶液中各种带电微粒的物质的量的浓度由大到小的顺序为c(NO3-)>c(NH4+)>c(Na+ )>c(OH-)>c(H+)
(3)A、C两元素的单质与熔融K2CO3组成的燃料电池,其负极反应式为H2+CO32--2e-=CO2↑+H2O用该电池电解1L 1mol/L NaCl溶液,当消耗标准状况下1.12L A2时,NaCl溶液的PH=13(假设电解过程中溶液的体积不变).
(4)25℃,两种酸的电离平衡常数如下表:
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
(5)常温下0.2mol/L的H2C2O4溶液的PH为2.1.H2C2O4与酸性高锰酸钾溶液反应,现象是有气泡(CO2)产生,紫红色消失.写出反应的离子方程式2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O又知该反应开始时速率较慢,随后大大加快,可能的原因是反应生成Mn2+对反应起到催化作用(忽略反应的热效应)
9.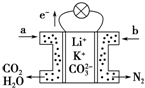 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图,下列说法正确的是( )
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图,下列说法正确的是( )
 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图,下列说法正确的是( )
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理如图,下列说法正确的是( )| A. | a为CH4,b为CO2 | |
| B. | CO32-向负极移动 | |
| C. | 此电池在常温时也能工作 | |
| D. | 正极电极反应式为O2+2H2O+4e-═4OH- |
16.一定温度下,在2.5L的恒容密闭容器中发生如下反应:CO2(g)+H2S(g)?COS(g)+H2O(g)
下列说法不正确的是( )
| 实验 | 温度/K | 起始物质的量/mol | 平衡物质的量/mol | 平衡常数 | |
| CO2 | H2S | H2O | |||
| Ⅰ | 607 | 0.11 | 0.41 | 0.01 | |
| Ⅱ | 607 | 0.22 | 0.82 | ||
| Ⅲ | 620 | 0.1 | 0.4 | 6.74×10-3 | |
| A. | 该反应正反应为吸热反应 | |
| B. | 607K时,把物质的量均为0.1mol四种反应物加入该反应器中,反应将向正反应方向进行 | |
| C. | 实验Ⅱ达到平衡时容器中COS的物质的量为0.02mol | |
| D. | 实验Ⅲ中,无论是开始还是至化学平衡状态,混合气体的密度始终不变 |
14.下列混合物的分离和提纯方法中,主要是从溶解性角度考虑的是( )
①过滤 ②蒸发 ③蒸馏 ④萃取.
①过滤 ②蒸发 ③蒸馏 ④萃取.
| A. | ①② | B. | ①④ | C. | ③④ | D. | ②③ |
 .
.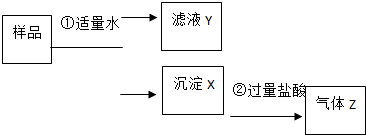 某固体物质是由NaOH、AlCl3、K2SO4、CaCO3、Ba(NO3)2 中的几种均匀混合而成,取样品进行如下实验(部分产物略去):
某固体物质是由NaOH、AlCl3、K2SO4、CaCO3、Ba(NO3)2 中的几种均匀混合而成,取样品进行如下实验(部分产物略去):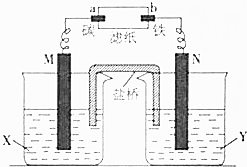 根据反应:Zn+CuSO4═Cu+ZnSO4设计原电池进行如图所示实验,滤纸上滴有酚酞和氯化钠溶液.实验进行一段时间后,在b电极附近出现红色.请回答下列问题:
根据反应:Zn+CuSO4═Cu+ZnSO4设计原电池进行如图所示实验,滤纸上滴有酚酞和氯化钠溶液.实验进行一段时间后,在b电极附近出现红色.请回答下列问题: