题目内容
19.X、Y、W、Q 四种元素在元素周期表中的位置如图,下列叙述错误的是( )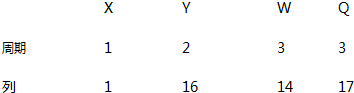
| A. | Y 的氢化物沸点高于 Q 的氢化物沸点 | |
| B. | 最高正价与最低负价之和为 0 的元素只有 W | |
| C. | 原子半径顺序为:r(W)>r(Q)>r(Y)>r(X) | |
| D. | X、Y、Q 三元素形成的分子中,原子最外层电子数之和最大为 32 |
分析 X位于第一周期第1列,则X为H元素;Y位于第二周期第16列,则Y位于第二周期Ⅵ族,为O元素;W位于第三周期第14列,则W位于第三周期IVA族,为Si元素;Q位于第三周期第17列,则Q位于第三周期ⅤⅡA族,为Cl元素,据此结合元素周期律知识解答.
解答 解:X位于第一周期第1列,则X为H元素;Y位于第二周期第16列,则Y位于第二周期Ⅵ族,为O元素;W位于第三周期第14列,则W位于第三周期IVA族,为Si元素;Q位于第三周期第17列,则Q位于第三周期ⅤⅡA族,为Cl元素,
A.Y的氢化物为水,Q的氢化物为HCl,由于水分子中存在氢键,则水的沸点大于HCl,故A正确;
B.X为H元素,其最高正价为+1,最低负价为-1,则X的最高正价与最低负价之和也为 0,故B错误;
C.电子层越多,原子半径越大,电子层相同时,核电荷数越大,原子半径越小,则原子半径:r(W)>r(Q)>r(Y)>r(X),故C正确;
D.H、O、Cl形成的化合物中,子最外层电子数之和最大的为HClO4,高氯酸分子中所有原子最外层电子数之和为:1+7+6×4=32,故D正确;
故选B.
点评 本题考查了原子结构与元素周期律的关系,题目浓度比,根据表中数据正确推断元素为解答关键,注意熟练掌握元素周期律内容、元素周期表结构,试题培养了学生的分析能力及逻辑推理能力.

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
9.下列各组微粒中,互为等电子体的一组是( )
| A. | CO、C2H2、N2 | |
| B. | SO2、NO${\;}_{2}^{+}$、N${\;}_{3}^{-}$、CNO- | |
| C. | CO${\;}_{3}^{2-}$、NO${\;}_{3}^{-}$、BeCl2 | |
| D. | SiF4、SiO${\;}_{4}^{4-}$、SO${\;}_{4}^{2-}$、PO${\;}_{4}^{3-}$ |
10.A和B是短周期元素,A2-和B+的核外电子总数之差为8,A的原子序数大于B,下列说法中正确的是( )
| A. | A和B的原子序数之差为8 | B. | A和B原子最外层电子数之和为8 | ||
| C. | A和B原子最外层电子数之和为3 | D. | A、B原子核外电子数总和可能为11 |
14.下列变化全部属于化学变化的是( )
| A. | 煤的干馏,石油分馏 | B. | 石油裂解,煤的气化 | ||
| C. | 金属导电,熔融氯化钠导电 | D. | 金属的焰色反应,浓硫酸吸水 |
8.人们常将在同一原子轨道上运动的、自旋方向相反的2个电子,称为“电子对”;将在同一原子轨道上运动的单个电子,称为“未成对电子”.以下有关主族元素原子的“电子对”和“未成对电子”的说法,错误的是( )
| A. | 核外电子数为奇数的基态原子,其原子轨道中一定含有“未成对电子” | |
| B. | 核外电子数为偶数的基态原子,其原子轨道中一定不含“未成对电子” | |
| C. | 核外电子数为偶数的基态原子,其原子轨道中一定含有“电子对” | |
| D. | 核外电子数为奇数的基态原子,其原子轨道中可能含有“电子对” |
3.能确定淀粉部分水解的试剂是( )
| A. | 碘液 | B. | 银氨溶液 | C. | 碘液和银氨溶液 | D. | 碘液或银氨溶液 |
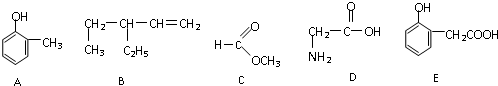
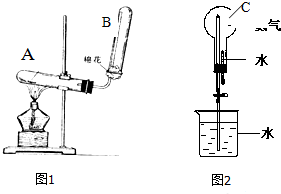 图(1、2)是有关氨的制取和性质的实验装置.
图(1、2)是有关氨的制取和性质的实验装置.