题目内容
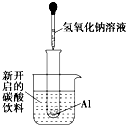 如图所示,把试管小心地放入盛有(20℃)碳酸饮料的烧杯中,试管中开始放入几小块铝片,再用滴管滴加5mL浓NaOH溶液于试管中,试回答下列问题:
如图所示,把试管小心地放入盛有(20℃)碳酸饮料的烧杯中,试管中开始放入几小块铝片,再用滴管滴加5mL浓NaOH溶液于试管中,试回答下列问题:(1)实验中观察到的现象是
(2)产生上述现象的原因是
(3)写出有关反应的离子方程式:
(4)由实验推知,反应所得溶液和氢气的总能量
考点:反应热和焓变
专题:化学反应中的能量变化
分析:金属与酸或碱溶液的置换反应是放热反应,铝与碱液的反应放热更为显著,放出的热量使烧杯中饮料的温度升高,使CO2溶解度减小,从而产生上述现象.根据反应的热效应与化学键的关系可知,放热反应中生成物的总能量小于反应物的总能量.
解答:
解:(1)铝与氢氧化钠溶液反应生成氢气并放出热量,溶液温度升高导致二氧化碳的溶解度减小,产生气体的速度加快,
故答案为:铝片上有大量气泡产生,铝片逐渐溶解;烧杯内液体放出气泡的速率加快;
(2)铝与氢氧化钠溶液反应生成氢气并放出热量,溶液温度升高导致二氧化碳的溶解度减小,产生气体的速度加快,
故答案为:铝与NaOH溶液反应生成氢气,且反应放热,碳酸饮料中CO2在水中的溶解度随温度升高而减小,CO2从饮料中逸出的速度加快
(3)铝与强碱反应时有水参与反应,反应的离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)反应放热说明生成物能量和小于反应物能量和,故答案为:小于.
故答案为:铝片上有大量气泡产生,铝片逐渐溶解;烧杯内液体放出气泡的速率加快;
(2)铝与氢氧化钠溶液反应生成氢气并放出热量,溶液温度升高导致二氧化碳的溶解度减小,产生气体的速度加快,
故答案为:铝与NaOH溶液反应生成氢气,且反应放热,碳酸饮料中CO2在水中的溶解度随温度升高而减小,CO2从饮料中逸出的速度加快
(3)铝与强碱反应时有水参与反应,反应的离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;
(4)反应放热说明生成物能量和小于反应物能量和,故答案为:小于.
点评:本题考查铝与氢氧化钠溶液的反应,该反应为放热反应,难度不大.要注意气体的溶解度随温度升高而减小.

练习册系列答案
相关题目