题目内容
对下列流程有关判断正确的是( )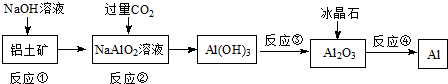

| A、流程中涉及的反应均为非氧化还原反应 |
| B、反应②产生的阴离子主要为CO32- |
| C、实验室中完成反应③应在蒸发皿中进行 |
| D、反应④的条件是电解熔融 |
考点:镁、铝的重要化合物
专题:元素及其化合物
分析:A、电解熔融Al2O3的反应属于氧化还原反应;
B、偏铝酸盐中通过量二氧化碳来获得氢氧化铝沉淀和碳酸氢钠;
C、加热分解氢氧化铝固体应在坩埚中进行;
D、反应④为电解熔融Al2O3制备铝单质.
B、偏铝酸盐中通过量二氧化碳来获得氢氧化铝沉淀和碳酸氢钠;
C、加热分解氢氧化铝固体应在坩埚中进行;
D、反应④为电解熔融Al2O3制备铝单质.
解答:
解:A、电解熔融Al2O3的反应属于氧化还原反应,反应的方程式为2Al2O3(熔融)
4Al+3O2↑,故A错误;
B、偏铝酸盐中通过量二氧化碳来获得氢氧化铝沉淀,即CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-,故B错误;
C、反应③为加热分解氢氧化铝固体应在坩埚中进行,故C错误;
D、反应④为电解熔融Al2O3制备铝单质,所以条件是电解熔融,故D正确.
故选D.
| ||
| 电解 |
B、偏铝酸盐中通过量二氧化碳来获得氢氧化铝沉淀,即CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-,故B错误;
C、反应③为加热分解氢氧化铝固体应在坩埚中进行,故C错误;
D、反应④为电解熔融Al2O3制备铝单质,所以条件是电解熔融,故D正确.
故选D.
点评:本题是一道综合知识题目,考查学生分析和解决问题的能力,综合性强,难度大.

练习册系列答案
相关题目
下列叙述正确的是 ( )
| A、红热的铜丝在氯气中剧烈燃烧,生成棕黄色的烟,加少量的水形成绿色溶液 |
| B、检验氨气的方法是将湿润的蓝色石蕊试纸靠近瓶口或管口,观察试纸是否呈红色 |
| C、在淀粉溶液中加入稀硫酸并加热数分钟,冷却后依次加入新制Cu(OH)2悬浊液和碘水可检验淀粉是否已发生水解和是否完全水解 |
| D、铁钉放试管中,加入2mL水、3滴稀醋酸和1滴K3[Fe(CN)6]溶液,不久铁钉周围出现蓝色溶液 |
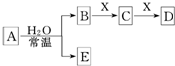 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去),下列推断不正确的是( )
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去),下列推断不正确的是( )| A、若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐 |
| B、若D为CO,C能和E反应,则A是Na2O2,X的同素异形体只有3种 |
| C、若A是单质,B和D的反应是OH-+HCO3-=H2O+CO32-,则E一定能还原Fe2O3 |
| D、若X是Na2SO3,C为气体,则A可能是氯气,且D和E能发生反应 |
关于Na2CO3与NaHCO3的性质判断正确的是( )
| A、常温下溶解度:Na2CO3<NaHCO3 |
| B、热稳定性:Na2CO3<NaHCO3 |
| C、与同浓度同体积的盐酸反应的速率:Na2CO3>NaHCO3 |
| D、与澄清石灰水反应,均有白色沉淀生成 |
将足量的铜片与100 ml 18 mol?L-1浓硫酸加热充分反应,收集到标准状况下的SO2气体V L,下列对此反应的有关说法中错误的是 ( )
| A、该反应体现了浓硫酸的酸性和强氧化性 | ||
| B、应体结束后两两种反应物均有剩余 | ||
C、被还原的硫酸为
| ||
| D、参加反应的Cu为0.9 mol |
现有乙烯、氯气和必要的试剂,若要在适当条件下制取1,1,2,2-四氯乙烷,则这一过程中所要经历的反应及耗用氯气的物质的量分别是(设乙烯的物质的量为1mol)( )
| A、取代,4 mol Cl2 |
| B、加成,2mol Cl2 |
| C、加成,取代,3 mol Cl2 |
| D、加成,消去,取代,3 mol Cl2 |

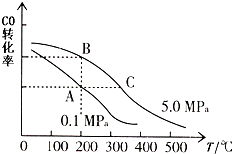 (1)在电化学中,常用碳作电极:
(1)在电化学中,常用碳作电极: