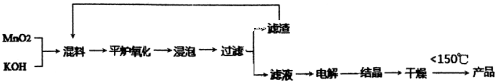
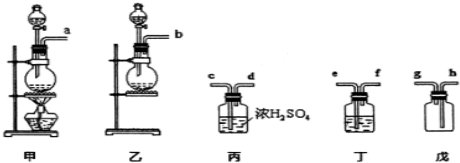
题目内容
小明同学非常喜欢实验探究课,为了探究SO2的相关性质做了下列实验,请根据下列情况回答相关问题.
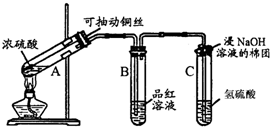
探究一:铜与浓硫酸反应产物的鉴定
(1)试管B中的实验现象是 .试管C中溶液变浑浊,则证明SO2具有 性.
(2)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是 ,如果浸NaHCO3溶液,则发生反应的化学方程式是 .
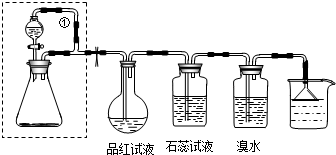
探究二:已知CO2和SO2的化学性质具有相似性和差异性.某同学为了确认干燥的SO2和Na2O2反应中是否有氧气生成吗,拟使用下列装置进行实验.
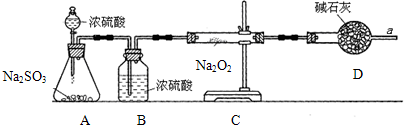
(3)D装置的作用是 .
(4)为确认SO2和Na2O2反应的产物,该同学设计了以下实验操作,你认为应该进行的操作(按先后顺序排列)是 (填序号).
A.用带火星的细木条靠近干燥管口a,观察细木条是否着火燃烧.
B.将C装置中反应后的固体物质溶于适量水配成溶液.
C.在配成的溶液中加入用硝酸(氧化性酸)酸化的硝酸钡溶液,观察是否有沉淀生成.
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成.

探究一:铜与浓硫酸反应产物的鉴定
(1)试管B中的实验现象是
(2)试管C口部的棉团既可浸碱溶液,又可浸NaHCO3溶液,其作用是
探究二:已知CO2和SO2的化学性质具有相似性和差异性.某同学为了确认干燥的SO2和Na2O2反应中是否有氧气生成吗,拟使用下列装置进行实验.

(3)D装置的作用是
(4)为确认SO2和Na2O2反应的产物,该同学设计了以下实验操作,你认为应该进行的操作(按先后顺序排列)是
A.用带火星的细木条靠近干燥管口a,观察细木条是否着火燃烧.
B.将C装置中反应后的固体物质溶于适量水配成溶液.
C.在配成的溶液中加入用硝酸(氧化性酸)酸化的硝酸钡溶液,观察是否有沉淀生成.
D.在配成的溶液中先加入盐酸,再加入氯化钡溶液,观察是否有气泡或沉淀生成.
考点:探究二氧化硫与水和品红溶液的反应
专题:实验题
分析:(1)二氧化硫与品红化合生成无色物质,能使品红溶液褪色;能和硫化氢发生氧化还原反应生成硫单质,证明SO2具有氧化性;
(2)从吸收二氧化硫,防止污染气体排放到大气中分析,结合NaHCO3溶液与二氧化硫的反应是利用亚硫酸酸性强于碳酸进行分析书写;
(3)根据浓硫酸、碱石灰的性质判断其作用;
(4)根据假设的产物确定实验步骤并检验生成物的成分.
(2)从吸收二氧化硫,防止污染气体排放到大气中分析,结合NaHCO3溶液与二氧化硫的反应是利用亚硫酸酸性强于碳酸进行分析书写;
(3)根据浓硫酸、碱石灰的性质判断其作用;
(4)根据假设的产物确定实验步骤并检验生成物的成分.
解答:
解:(1)装置B中装有品红溶液,实验过程中,二氧化硫与品红化合生成无色物质,品红溶液褪色;硫化氢和二氧化硫反应生成硫单质,硫不易溶于水,所以看到无色溶液中出现淡黄色沉淀,二氧化硫得电子而作氧化剂,氧化剂具有氧化性,
故答案为:品红溶液褪色;氧化;
(3)试管C口部的棉团浸NaHCO3溶液,是利用碳酸氢钠溶液的碱性和酸性氧化物二氧化硫反应,吸收污染气体,防止污染大气,反应的化学方程式为NaHCO3+SO2=NaHSO3+CO2 (或2NaHCO3+SO2=Na2SO3+2CO2↑+H2O),
故答案为:尾气处理;NaHCO3+SO2=NaHSO3+CO2 (或2NaHCO3+SO2=Na2SO3+2CO2↑+H2O);
(3)浓硫酸有吸水性,能吸收二氧化硫中的水分,防止水蒸气与过氧化钠反应而干扰二氧化硫;碱石灰是干燥剂,能吸收水分,防止水蒸气的干扰;碱石灰是碱性物质,能吸收二氧化硫等酸性气体,防止污染大气,
故答案为:除去空气中的CO2和水蒸气,以免对实验造成干扰;
(4)A.用带火星的木条可检验氧气,故A正确;
B.C装置中反应后的物质是固体,先把固体物质溶于适量水配成溶液,实验时反应速率快、现象更明显,故B正确;
C.硝酸有强氧化性,能把亚硫酸根离子氧化成硫酸根离子,会干扰硫酸根离子的检验,故C错误;
D.盐酸有弱氧化性,不能把亚硫酸根离子氧化成硫酸根离子,且能除去亚硫酸根离子,然后加入氯化钡观察是否有气泡或沉淀生成,从而确定固体成分,故D正确;
故选ABD.
故答案为:品红溶液褪色;氧化;
(3)试管C口部的棉团浸NaHCO3溶液,是利用碳酸氢钠溶液的碱性和酸性氧化物二氧化硫反应,吸收污染气体,防止污染大气,反应的化学方程式为NaHCO3+SO2=NaHSO3+CO2 (或2NaHCO3+SO2=Na2SO3+2CO2↑+H2O),
故答案为:尾气处理;NaHCO3+SO2=NaHSO3+CO2 (或2NaHCO3+SO2=Na2SO3+2CO2↑+H2O);
(3)浓硫酸有吸水性,能吸收二氧化硫中的水分,防止水蒸气与过氧化钠反应而干扰二氧化硫;碱石灰是干燥剂,能吸收水分,防止水蒸气的干扰;碱石灰是碱性物质,能吸收二氧化硫等酸性气体,防止污染大气,
故答案为:除去空气中的CO2和水蒸气,以免对实验造成干扰;
(4)A.用带火星的木条可检验氧气,故A正确;
B.C装置中反应后的物质是固体,先把固体物质溶于适量水配成溶液,实验时反应速率快、现象更明显,故B正确;
C.硝酸有强氧化性,能把亚硫酸根离子氧化成硫酸根离子,会干扰硫酸根离子的检验,故C错误;
D.盐酸有弱氧化性,不能把亚硫酸根离子氧化成硫酸根离子,且能除去亚硫酸根离子,然后加入氯化钡观察是否有气泡或沉淀生成,从而确定固体成分,故D正确;
故选ABD.
点评:本题考查了常见气体的制取和实验装置的选择,侧重考查了SO2的性质的实验设计和性质分析判断,掌握二氧化硫酸性氧化物性质、漂白性、还原性等是解题关键,题目难度中等.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
 25℃时,在25mL0.1mol/L的氢氧化钠溶液中,逐滴加入0.2mol/LCH3COOH,溶液的pH的变化曲线如图所示,下列分析的结论正确的是( )
25℃时,在25mL0.1mol/L的氢氧化钠溶液中,逐滴加入0.2mol/LCH3COOH,溶液的pH的变化曲线如图所示,下列分析的结论正确的是( )| A、若B点的横坐标a=12.5,且有c(Na+)=c(CH3COO-) |
| B、对曲线上A、B间任何一点,溶液中都有:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| C、D点时,c(CH3COO-)+c(CH3COOH)=c(Na+) |
| D、C点时,c(CH3COO-)=c(Na+)>c(H+)=c(OH-) |
下列溶液中各微粒的浓度关系一定正确的是( )
| A、某酸性溶液中只含NH4+、Cl-、H+、OH-四种离子,溶液中一定存在:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B、物质的量浓度相同的4种溶液:①CH3COONa;②NaNO3;③Na2CO3;④NaOH,pH的大小顺序是:④>③>①>② |
| C、在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
| D、25℃时,pH=10的CH3COONa溶液与pH=10的氨水中,由水电离出的c(OH-)之比为1:1 |
下列叙述正确的是( )
| A、0.1mol/L NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+c(HCO3-)+c(CO32-) |
B、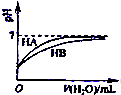 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液PH随加水量的变化,则NaA溶液的PH大于同浓度的NaB溶液的PH |
C、 表示在其他条件相同时,分别在T1、T2温度下由CO2和H2合成甲醇的物质的量随时间变化情况,则CO2和H2合成甲醇是放热反应 |
D、 表示将1.000 mol/L氨水滴入20.00mL1.000 mol/L盐酸中,溶液PH和温度随加入氨水体积变化曲线 |
下列关于常见有机物的说法中,不正确的是( )
| A、甲烷、苯、乙醇和乙酸在一定条件下都能发生取代反应 |
| B、乙烯使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色的反应类型不同 |
| C、塑料、合成橡胶、合成纤维都属于合成有机高分子材料 |
| D、化学式均为(C6H10O5)n的淀粉和纤维素互为同分异构体 |
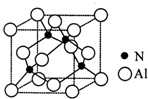 氮的化合物在无机化工领域有着重要的地位.请回答下列问题:
氮的化合物在无机化工领域有着重要的地位.请回答下列问题: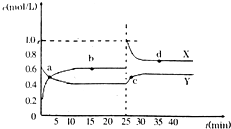 有关元素A、B、C、D的信息如下:
有关元素A、B、C、D的信息如下: